СИЛІКАТИ — широкий клас сполук, утворених діоксидом кремнію (кремнеземом) і оксидами інших елементів. С. — найважливіший клас мінералів, який нараховує понад 500 представників, що становлять 75% від маси земної кори. Третина відомих науці мінералів належить до класу силікатів та алюмосилікатів. Різноманіття С. пов’язане зі здатністю атомів кремнію з’єднуватися між собою через атоми кисню, утворюючи, залежно від природи оксидів металів і їх співвідношення з оксидом кремнію, кремнієвокисневі радикали різної будови та ізоструктурно заміщатися на атоми Al, B, Be та інші, відповідно до чого розрізняють алюмо-, боро-, берило- та інші силікати. С. можуть мати як природне, так і синтетичне походження. За хімічною природою С., і особливо складні С., належать до типових гетеросполук, в яких реалізуються водночас різні багатоцентрові типи хімічних зв’язків: іонний, ковалентний, іонно-ковалентний, координаційний, водневий та ін. В основі будови кристалічних решіток будь-якого С. знаходиться так званий кремнієвокисневий тетраедр (рисунок), тобто атом кремнію, сполучений із чотирма атомами кисню.
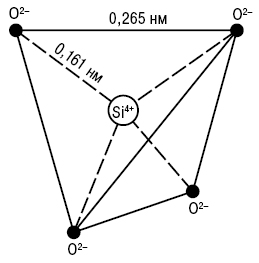
Рисунок. Елементарний правильний кремнієвокисневий тетраедр SiO44-
Різноманітність способів з’єднання цих тетраедрів один з одним є підставою поділу С. на два класи: острівні та полімерні, або конденсовані. До острівних належать олівін, циркон, титаніт, топаз, дистен, андалузит, ставроліт, везувіан, каламін, епідот, цоізит, ортит, родоніт, берил, кордієрит, турмалін та ін. Клас конденсованих С. містить чотири підкласи: ланцюгові (піроксени ромбічні (енстатит, гіперстен) і моноклінні (діопсид, саліт, геденбергіт, авгіт, егерин, сподумен, воластоніт, силіманіт)), стрічкові (тремоліт, актиноліт, жадеїт, рогова обманка), шаруваті або листові (тальк, серпентин, хризотил-азбест, ревдинскіт, полігорскіт, слюди (мусковіт, флогопіт, біотит), гідрослюди (вермікуліт, глауконіт), хлорити (пеніт, клинохлор та інші), мінерали глин (каолініт, хризокола, гарнієрит та ін.), мурманіт та каркасні (кальцієво-натрієві польові шпати або плагіоклази (альбіт, oлігoклaз, андезин, лaбpaдop, бітoвніт, aнopтит), калієво-натрієві польові шпати (opтoклaз, aнopтoклaз), фельдшпатоїди (нефелін, лейцит)). Окремі мінерали виділяються за складом катіонів, компенсуючих негативний заряд кремнієвокисневого тетраедра, а також за ступенем заміщення кремнію на алюміній.
Як правило, С. є тугоплавкими і хімічно пасивними речовинами, погано або практично нерозчинними у воді. Залежно від температури вони можуть знаходитись у газоподібному, рідкому (розплавленому) і твердому стані, а також утворювати високодисперсні (колоїдні) системи з розміром частинок 10–6–10–9 м, в яких є поверхня розділу між частинками силікатів і дисперсійним середовищем.
Найбільш розповсюдженими є алюмосилікати, які мають каркасну будову та загальну формулу (AlmSin-mO2n)m-. Надлишковий від’ємний заряд аніонного остова із (Al,Si)-тетраедрів електростатично компенсується лужними та лужноземельними катіонами, що розташовані в порожнинах каркасної структури. Серед каркасних алюмосилікатів більш за все в природі поширені лужні польовошпатові С.: тверді розчини альбіту NaAlSi3O8 та ортоклазу KAlSi3O8, а також альбіту та анортиту CaAl2Si2O8, відомі під назвою плагіоклазів. Каркасні С. цеоліти характеризуються великими внутрішніми порожнинами та вхідними вікнами, в яких можуть адсорбовуватися молекули діаметром 2,6–8 Å. Ізоморфне заміщення кремнію на алюміній обумовлює виражені кислотні властивості тетраедричного Al в алюмокремнієвокисневих аніонних групах та основні властивості в октаедричній координації.
Алюмосилікати, які містять молекули води, отримали назву алюмогідросилікатів (монтморилоніт, нонтроліт, гідрослюда, каолініт (основна речовина глини медичної білої), галуазит та ін.). Більшість з них володіє добре вираженими колоїдно-хімічними властивостями (пептизація, коагуляція, адсорбція, обмін іонів та ін.).
С. здавна використовуються народною медициною як речовини для знешкодження отрут, подразників шлунка та кишечнику, запальних виділень в організмі, а також зовнішньо — для поглинання ексудату та як підсушувачі. На сьогодні у фармації С. використовують як основу для приготування паст, мазей, таблеток, пілюль, а мінерали — як зв’язувачі (див. Іммобілізація) для нестійких АФІ та як сорбенти (для поглинання шкідливих речовин в організмі). Змінюючи рН реакційного середовища, можна легко змінювати в потрібному напрямі властивості глинистих мінералів і одержувати С. з малою або великою питомою поверхнею та гідрофільністю, різним значенням до набухання, гелеутворення, а також пористістю. Так, для збереження кислого середовища шкіри в присипках і мазях використовують водневу форму С.; у пілюлях з калію перманганатом — бентоніт з каолінітом; з речовинами, що спікаються при пресуванні таблеток, — галуазит з полігорскитом; в емульсійних системах типу олія/вода (о/в) — гідрофільні мінерали, типу вода/олія (в/о) — органофільні модифіковані мінерали. Алюмосилікати як дисперсні мінерали використовують при виготовленні порошків для внутрішнього застосування, як стабілізатори водних та олійних емульсій — у кремах, гелях, мазях, пастах, супозиторіях, драже, таблетках і в технології виготовлення настоянок, екстрактів, сиропів, культуральних рідин, вакцин та ін.
С. широко застосовують також як складові компоненти при виготовленні скла, цементу, будівельної кераміки, цегли. Природні С. є сировиною при виробництві Li, Al, Be, Cs, Zr, Hf, соди та поташу. С. лужних металів використовують у виробництві клею, фарб, мастил та мила. Природні та синтетичні С. використовують як адсорбенти та матеріали з іонообмінними властивостями.
Сало Д.П., Овчаренко Ф.Д., Круглицкий Н.Н. Высокодисперсные минералы в фармации и медицине. — К., 1969; Химическая энциклопедия: В 5 т. / Редкол. Н.С. Зефиров (гл. ред.) и др. — М., 1995. — Т. 4.
