ОСМОС (грец. ôsmos — поштовх, тиск) — самодовільний процес проникнення через напівпроникну мембрану розчинника з розчину нижчої концентрації у розчин із вищою концентрацією, зумовлений вирівнюванням хімічних потенціалів розчинника. Розглянемо два бінарних розчини — α і β (рисунок), розділених напівпроникною перегородкою, яка пропускає молекули розчинника (компонент 1) і не пропускає молекули розчиненої речовини (компонент 2).
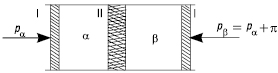
Рисунок. Схема встановлення осмотичної рівноваги в розчинах, розділених напівпроникною мембраною: І — поршні, якими можна регулювати тиск на бінарні розчини α і β; ІІ — напівпроникна мембрана
Якщо температура Т і тиск р з обох боків мембрани однакові (Tα=Tβ, рα=рβ), а молярні частки розчинника різні (xα1>xβ1), то його хімічні потенціали також відрізнятимуться µα1 (T, р, xα1)> µβ1 (T, р, xβ1). За такої умови система буде термодинамічно нерівноважною, тому компонент 1 переходитиме із об’єму α в об’єм β, доки його молярні частки в обох об’ємах не стануть однаковими. Для запобігання масоперенесенню та вирівнюванню концентрацій і для збереження вихідного складу обох розчинів необхідно зрівняти хімічні потенціали компонента 1 з обох боків мембрани зміною зовнішніх умов (температури, тиску тощо). В ізотермічних умовах для збереження складу фаз необхідно змінити тиск на один із розчинів. Додатковий тиск π=рβ–рα, який слід прикласти до розчину α, щоб у нього не переходив розчинник через напівпроникну мембрану з розчину α, називається осмотичним тиском. Про методи і техніку вимірювання осмотичного тиску див. О. При тиску рβ=рα+π система знаходитиметься у термодинамічній рівновазі. Якщо рβ–рα>π, рівновага порушується і розчинник переходитиме із більш концентрованого розчину в менш концентрований. Це явище назвали зворотним О. Залежність осмотичного тиску, розбавленого бінарного розчину від молярної концентрації розчиненої недисоціюючої речовини с2, виражається рівнянням Вант-Гоффа:
π=c2RT, (1)
де R — газова стала; T — температура.
Для розбавлених розчинів електролітів рівняння Вант-Гоффа має вигляд:
π=іс2RT, (2)
де і — ізотонічний коефіцієнт Вант-Гоффа (див. Ізотонічний коефіцієнт (коефіцієнт Вант-Гоффа)).
Явище О. відіграє велику роль у процесах життєдіяльності різних організмів. Внутрішньоклітинний тиск зумовлює тургор клітин, тобто міцність і пружність тканин. Локальні зміни осмотичного тиску тканинних рідин можуть бути досить значними, напр. при запальних процесах відбувається розпад білків. Як наслідок збільшується кількість структурних частинок у вогнищі запалення та значно підвищується в ньому осмотичний тиск, що спричиняє виникнення набряків внаслідок локального відтоку води з навколишніх тканин. Кров, лімфа та інші рідини організму людини мають сталий осмотичний тиск, приблизно 8•105 Па при температурі 37 °С. Такий самий осмотичний тиск має 0,9% розчин хлориду натрію. Розчини, що мають однакові осмотичні тиски, називають ізотонічними або ізоосмотичними. Однією з основних вимог до ряду лікарських форм (очні краплі, інфузійні розчини тощо) є їх ізотонічність внутрішньоклітинним рідинам організму людини. У більш розбавлених розчинах (гіпотонічних) клітини набрякають і лопаються (явище лізису). Напр. еритроцити, поміщені в гіпотонічний розчин, руйнуються й забарвлюють його в червоний колір (явище гемолізу). У концентрованих розчинах (гіпертонічних) клітини зморщуються (явище плазмолізу). У медичній практиці застосовують і гіпертонічні розчини, напр. при лікуванні пацієнтів з артеріальною гіпертензією, яка супроводжується порушенням мозкового кровообігу, для в/в ін’єкцій використовують 40% розчин глюкози. У хірургії гіпертонічні пов’язки — марлю, змочену в гіпертонічному розчині NaCl, — вводять у рани; при цьому ранова рідина рухається назовні по марлі, а рана очищується від мікроорганізмів, гною тощо.
Явище О. покладено в основу розроблення осмотичних терапевтичних систем різних конструкцій — перспективних ЛП із регульованим виділенням лікарських речовин, які знайшли застосування в медицині. За допомогою таких систем можна вводити (перорально чи іншим способом) ліки, які мають протизапальну, судинорозширювальну, жарознижувальну чи іншу дію.
Зворотний О. застосовується в мембранних процесах розділення речовин для одержання надчистої води, для очищення стічних вод, рідких радіоактивних відходів, опріснювання морської води тощо. У фармацевтичній і мікробіологічній промисловості зворотний О. включають у технологічний цикл при виробництві та виділенні БАР, антибіотиків, гормонів, вітамінів, вакцин, ферментів тощо.
Брык М.Т., Цапюк Е.А., Твердый А.А. Мембранная технология в промышленности. — К., 1990; Духин С.С., Сидорова М.П., Ярощук А.Э. Электрохимия мембран и обратный осмос. — Л., 1991; Дытнерский Ю.И. Обратный осмос и ультрафильтрация. — М., 1978; Фізична і колоїдна хімія / В.І. Кабачний, Л.К. Осіпенко, Л.Д. Грицан. — Х., 1999; Химическая энциклопедия: В 5 т. — М., 1992. — Т. 3.
