Ліпіди (грец. lipos — жир) — велика група природних гідрофобних сполук, неоднорідних за хімічним складом і біологічними функціями, які об’єднують за такими критеріями: 1) обмежена розчинність у воді та полярних розчинниках і, навпаки, хороша розчинність у неполярних розчинниках; 2) знаходження в природі у вигляді складних ефірів вищих жирних кислот; 3) наявність в усіх живих організмах.
Деякі ліпіди (жири тваринні, рослинні) використовують здавна як продукти харчування, для виготовлення ліків і косметики, а також для освітлення приміщень. З початку XVIII ст. Ліпіди стали використовувати для миловаріння, а з XX ст. — для виробництва мийних засобів, емульгаторів, детергентів, пластифікаторів і технологічних мастил. Перший елементний аналіз Л. виконав А. Лавуазьє на початку XIX ст., а перші дослідження хімічної будови належать К. Шеєле і М. Шевролю. Фосфоліпіди виділив М. Гоблі у 1847 р. Досі вже була відома будова найважливіших жирних кислот. Термін «Ліпіди» був запропонований В. Блуром і згідно з його класифікацією, модифікованою E. Масоро, існують прості та складні Л. Унаслідок лужного або кислотного гідролізу прості Л. не розщеплюються і не розкладаються з утворенням ліпідних дериватів, які зберігають притаманну ліпіди розчинність в органічних розчинниках. Подальшу історію вивчення ліпідів можна поділити на три періоди, що різняться за методами дослідження. На першому етапі (1880–1950) використовували традиційні методи органічної хімії. Другий етап (1950–1970) характеризується застосуванням хроматографічних методів. З’явилися спеціалізовані наукові журнали, обсяг публікацій сягає тисяч щорічних статей. Фізико-хімічні методи (мас-спектроскопія, оптична спектроскопія, радіоспектроскопія, флуоресцентний аналіз тощо) зробили у 70–80 рр. ХХ ст. прорив у вивченні тонкої структури ліпідів. Вивченням і систематизацією ліпідів займалися Т.П. Гільдич і Г.С. Джеймсон. Дослідження з хімії й технології жирів за часів радянської влади були сконцентровані у Всесоюзному науково-дослідному інституті жирів, його філіях, у Московському технологічному інституті харчової промисловості, у Краснодарському, Ташкентському і Харківському політехнічних університетах.
Ліпіди класифікують:
- за функціями, які вони виконують в організмі, виділяють ліпіди запасні та мембранні (фосфоліпіди та гліколіпіди);
- за фізичними властивостями — нейтральні (неполярні) та полярні;
- за хімічними властивостями — ліпіди , які омилюються лугами (жири, віск, складні ліпіди), та неомилювані ліпофільні речовини.
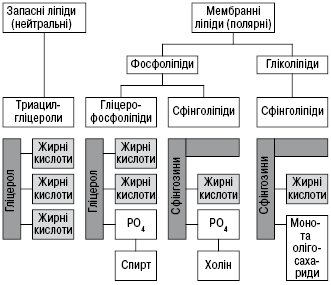
Сучасна класифікація поділяє ліпіди на прості та складні, окремі групи становлять похідні і різні ліпіди. Прості ліпіди — це ефіри жирних кислот із різноманітними спиртами (див. Вищі жирні кислоти). До них належать жири, або ацилгліцероли (ефіри жирних кислот і гліцеролу), воски, а також ефіри холестеролу і вищих жирних кислот. Складні ліпіди — це ефіри жирних кислот і спиртів, гідроксильні групи яких містять інші замісники. До цієї групи належать фосфоліпіди, гліколіпіди, сфінголіпіди, ліпопротеїди, ліпополісахариди (див. Гліколіпіди, Ліпопротеїди). Похідні ліпіди — сполуки, які утворюються внаслідок гідролізу складних ліпідів, тобто вищі жирні кислоти, моно- та діацилгліцероли, гліцерол (див. Гліцерин), стерини (див. Стероїди), жирні альдегіди, ліпідна частина ліпопротеїдів. До групи різних ліпідів належать аліфатичні вуглеводні, сквален, інші терпени, вітаміни Е, К, ефіри гліцеролу, глікозилгліцероли тощо. Іноді сполуки, подібні до ліпідів за фізико-хімічними властивостями, називають ліпоїдами (фосфоліпіди, воски, стероїди, у т.ч. холестерол та його ефіри, біологічно активні гормони і жовчні кислоти). Усі ліпіди умовно можна поділити на неполярні (нейтральні) та полярні; ліпіди, що омилюються лугами (жири, воски, складні Л.), і неомилювані (ізопреноїди, каротиноїди, простагландини тощо). За ліпофільними властивостями до ліпідів іноді зараховують терпеноїди, стероїди, каротиноїди, а також хлорофіл. Певною мірою віднесення цих сполук до ліпідів виправдано, оскільки всі вони в живих організмах разом знаходяться із Л. і екстрагуються органічними розчинниками.
Хімічна структура ліпідів різноманітна (табл. 1–3). Воски мають рослинне, тваринне і мінеральне походження (див. Віск). Вони належать до нейтральних ліпідів, є складними ефірами жирних кислот і жирних спиртів, мають загальну формулу
![]() ,
,
де R1, R2 — алкільний або алкенільний радикали. У нейтральних гліцероліпідах групи ОН гліцеролу заміщені залишками вищих жирних кислот, аліфатичних спиртів або альдегідів. Гліцероли, або гліцероліпіди, є основними компонентами жирів. Жири становлять самостійну групу ліпідів (див. Жири). Вони є сумішшю ацилгліцеролів із речовинами ліпідного і неліпідного характеру. Останні у кількості 3–5% супроводжують ацилгліцероли у природних жирах. Відмінною особливістю плазмалогенів є наявність вінільно-ефірного угруповання –О–СН=СН–. Унаслідок гідролізу вони утворюють довголанцюгові альдегіди, які називають плазмолями. До нейтральних гліколіпідів належать речовини, які мають ковалентносполучені ліпідний та вуглеводний компоненти, напр. моно- і дигалактозилгліцероли, виділені з рослинних, тваринних тканин і мікроорганізмів. У складі гліколіпідів бактерій ідентифіковані також глюкоза, арабіноза, маноза, рамноза, трегалоза.
Таблиця 1. Структура нейтральних ліпідів
Гліцероли (гліцероліпіди, ацилгліцероли, нейтральні жири) (R1, R2, R3 — ацил або Н)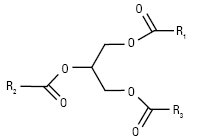 |
| Плазмалогени, або алкенільно-ефірні нейтральні Л. (R1 — алкеніл, R2, R3 — ацили) Алкілдіацилгліцероли (R1– алкіл, R2, R3 — ацили) 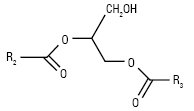 |
Діольні Л. (R1, R2 — ацил, алкіл або алкеніл, n=0–4)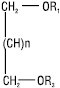 |
Фосфоліпіди — полярні гліцероліпіди, в яких дві гідроксильні групи гліцеролу заміщені вищими жирними кислотами, а третя зв’язана із залишком ортофосфатної кислоти (вільної чи етерифікованої холіном, етаноламіном або міоінозитом) або залишком сахаридів (глікозилдигліцериди). Їх поділяють на фосфогліцероли, фосфосфінголіпіди, фосфоноліпіди, діольні фосфоліпіди і амінокислотні ефіри фосфатидилгліцеролу (див. Фосфоліпіди).
У тканинах живих організмів фосфоліпіди виконують такі функції:
- структурні компоненти мембран;
- активатори ензимів;
- компоненти сурфактанту легенів;
- джерела арахідонової кислоти (попередника ейкозаноїдів), месенджерів (діацилгліцеролу та інозитолтрифосфату);
- беруть участь у формуванні транспортних форм інших ліпідів;
- можуть виконувати енергетичну функцію.
Таблиця 2. Структура гліцерофосфоліпідів
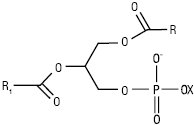 |
R, R1=ацил, алкіл або алкеніл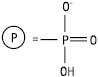 – залишок фосфатної кислоти – залишок фосфатної кислоти |
|
| Х = Н | Фосфатидні кислоти | |
| R1 = Н | Лізофосфоліпіди | |
| Х = холін | 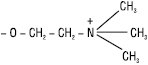 |
Фосфатидилхоліни (лецитини) |
| Х = етаноламін | 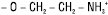 |
Фосфатидилетаноламіни (кефаліни) |
| Х = серин | 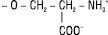 |
Фосфатидилсерини |
| Х = інозит | 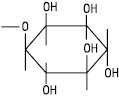 |
Фосфатидилінозити (інозитиди) |
| Х = гліцерол | 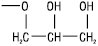 |
Фосфатидилгліцероли |
| Х = фосфатидилгліцерол | 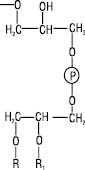 |
Кардіоліпіни |
| Х = етаноламін або холін R з угрупованням –О–СН = СН– | Плазмалогенні фосфоліпіди | |
Положення радикалів у молекулі гліцероліпідів позначають за стереоспецифічною нумерацією: якщо у фішеровській проекції вторинний гідроксил гліцеринового залишку знаходиться зліва (β-положення), то атоми вуглецю, розташовані вище або нижче цієї групи, позначаються індексами sn і номерами 1 і 3 (або буквами α та α1), напр. sn-1-ацил-3- гліцерофосфохолін.
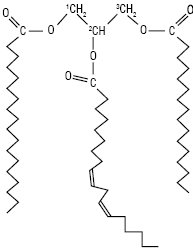
Пальмітлінолілгліцерол
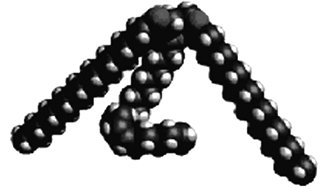
У водних середовищах ліпіди утворюють бішарові, гексагональні або міцелярні структури. У ліпідному бішарі насичені вуглеводневі ланцюги зазвичай знаходяться в зиґзаґоподібній конформації й розташовані паралельно один до одного. Вісь sn-1-ацильного ланцюга збігається з віссю гліцеринового залишку, тоді як sn-2-ланцюг на початковій –СО–СН2-ділянці відходить від гліцеринового залишку під прямим кутом і, різко згинаючись біля α-вуглецевого атома, стає далі рівнобіжним sn-1-ланцюга. Ненасичені вуглеводневі ланцюги Л. містять один або кілька етиленових зв’язків, які зазвичай мають цис-конфігурацію. За наявності подвійних зв’язків зиґзаґоподібна конформація порушується. У молекулах цвітер-іонних фосфоліпідів (напр. фосфатидилхоліну і фосфатидилетаноламіну) полярне угруповання («голівка») розташоване перпендикулярно до осей ацильних ланцюгів, а в молекулах негативно заряджених фосфоліпідів (напр. фосфатидилсерину) полярні голівки спрямовані паралельно осі ацильних ланцюгів. Структурною основою сфінголіпідів (див. табл. 3) є N-ацильні похідні сфінгозинових основ, тому сфінголіпіди можна розглядати як цераміди із заміщеним первинним гідроксилом. Сфінгозинові основи різняться довжиною вуглецевих ланцюгів, ступенем насиченості, кількістю гідроксильних груп (див. Сфінголіпіди).

У фосфосфінголіпідів осі ацильних ланцюгів і сфінгозинового залишку також розташовані паралельно один до одного. Іншу просторову структуру мають глікосфінголіпіди, які разом з іншими сфінголіпідами є важливими компонентами клітинних мембран усіх органів і тканин людини і тварин. Цереброзиди, гангліозиди і сульфоліпіди містять у структурі вуглеводні залишки і належать до полярних гліколіпідів. У цереброзидів рівнобіжне розташування аліфатичних ланцюгів забезпечується внаслідок вигинів ланцюга сфінгозину при першому і шостому атомах С, а кільце залишку моносахариду орієнтоване майже перпендикулярно до вуглеводневих ланцюгів. У глікосфінголіпідів з олігосахаридним ланцюгом останній орієнтований переважно за напрямком осей вуглеводневих ланцюгів.
Таблиця 3. Структура сфінголіпідів і гліколіпідів
| Сфінгозин, R = алцил, алкіл або алкеніл 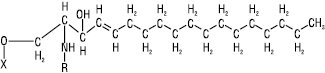 |
|||
| СФІНГОЛІПІДИ | Х = Н | Цераміди | |
| Х = фосфохолін | Сфінгомієліни | ||
| Залишки нейтрального моно- чи олігосахариду | Цереброзиди | ГЛІКОЛІПІДИ | |
| Олігосахаридний ланцюг, який містить залишки сіалових кислот | Гангліозиди | ||
| Сульфосахариди: Glu–SO3H Gal–SO3H |
Сульфоліпіди | ||
Полярні ліпіди є амфіфілами (грец. amphi — обидва і phyle — спорідненість), оскільки містять замісники двох типів: гідрофільні групи фосфорної кислоти та азотистої основи («голова») і гідрофобні неполярні вуглеводневі радикали («хвости»). Полярні ліпіди здатні відповідним чином розташовуватися на межі розподілу двох фаз, завдяки чому утворюється ліпідний бішар мембран (див. Мембрани біологічні). Таким чином, ліпіди є в усіх живих організмах. Вміст ліпідів у мембранах і структурних компонентах клітини відносно стабільний і знижується лише в патологічних станах, які надалі викликають руйнування клітини. Фосфоліпіди становлять 30–35% маси типової біомембрани. З фізіологічних позицій структурні ліпіди є обов’язковими постійними компонентами протоплазми (протоплазматичними), на противагу резервним Л. Запасними ліпідами рослин є триацилгліцероли, що утворюються з ацетил-КоА, накопичуються у сім’ядолі жирозапасливого насіння при його дозріванні і згодом стають основними ліпідними компонентами харчування людини. Вони містяться в рослинних тканинах у спеціальних органелах, що одержали різні назви: сферосоми, олеосоми або жирові тільця. Жири розщеплюються при проростанні насіння, перетворюючись на вуглеводи, якими живиться зародок.
Ацилгліцероли, фосфоліпіди і холестерол входять до складу клітин усіх тканин, інші Л. специфічні, напр. цереброзиди для мозкової тканини. Вміст ліпідів у різних органах і тканинах людини неоднаковий. Якщо не брати до уваги жирову тканину, найбільше ліпідів знаходиться у нервовій тканині, де їх вміст становить 51–54% маси сухої речовини. Нервова тканина найбагатша на фосфоліпіди і сфінгомієліни (28% сухої маси), холестерол (10%), цереброзиди і гангліозиди (7%). У печінці людини міститься 7–14% Л. При жировій дистрофії печінки вміст ліпідів у тканині органа сягає 45% сухої маси, головним чином, за рахунок збільшення кількості триацилгліцеролів (табл. 4).
Таблиця 4. Вміст ліпідів у плазмі крові людини
| Клас Л. | Вміст, мг% |
| Неетерифіковані жирні кислоти | 8–20 |
| Триацилгліцероли | 50–200 |
| Фосфоліпіди | 110–275 |
| Сфінгомієліни | 30–60 |
| Холестерол неетерифікований | 50–110 |
| Холестерол етерифікований | 100–220 |
Організм людини щодня метаболізує близько 1 г холестеролу, з якого половина потрапляє з їжею. Холестерол — стабілізуюча складова біологічних мембран і вихідний матеріал для синтезу стероїдних гормонів. Він є найважливішим прекурсором жовчних кислот. Поширення фосфоліпідів у специфічних клітинах різне. Плазмалогени становлять 25–30% (іноді понад 50%) загального вмісту фосфоліпідів. Вміст фосфатидових кислот і фосфатидилгліцеринів у клітинах невеликий; кількість фосфатидилхолінів може сягати 45–50% загального вмісту ліпідів клітини; фосфатидилетаноламіни входять до складу клітин і субклітинних структур у кількості 30–40% від усіх фосфоліпідів; фосфатидилсерини є обов’язковим компонентом суміші фосфоліпідів (близько 5%); кардіоліпіни, вперше виділені у 1941 р. з міокарда, поширені у природі, але їх вміст невеликий; у внутрішньоклітинних структурах концентруються у мітохондріях, завдяки чому їх розглядають як хімічний маркер мітохондрій; поліфосфоїнозити накопичуються у тканинах головного мозку. Тварини здатні синтезувати всі основні класи Л. або ресинтезувати їх з продуктів розпаду харчових Л. Не синтезуються в організмі тварин і людини жиророзчинні вітаміни та незамінні поліненасичені жирні кислоти. Метаболізм Л. складається з перетравлення і всмоктування Л., окиснення жирних кислот, біосинтезу жирних кислот, синтезу складних Л., біосинтезу стероїдів, транспортування Л. Близько 40% жирів, що надійшли з їжею, розщеплюються в тонкому кишечнику і всмоктуються у вигляді гліцеролу і жирних кислот. 3–10% триацилгліцеролів усмоктуються без змін структури, інші ліпіди — у вигляді моногліцеролів. При цьому жирні кислоти з ланцюгом менше С10 проникають у капіляри портальної вени і надходять безпосередньо в печінку. Жирні кислоти з більшою довжиною вуглецевого ланцюга надходять у лімфатичні капіляри у складі триацилгліцеролів, вбудовуються в хіломікрони і надходять у кров із лімфою через лімфатичні судини. Перетравлення нейтральних Л. відбувається у дванадцятипалій кишці, куди надходить ліпаза, кон’юговані жовчні кислоти і білковий кофактор, названий коліпазою. Ліпази підшлункової залози відщеплюють жирні кислоти тільки від α- і α1-атомів гліцеролів, а ліпази кишечнику також і від β-атома. Жирні кислоти, що вивільнилися, розпадаються далі за рахунок β-окиснення до ацетил-КоА, що, в свою чергу, окиснюється у циклі лимонної кислоти або транспортується в цитоплазму, де бере участь у синтетичних реакціях. Гліцерол розпадається в послідовних реакціях гліколізу.
Крім того, існує п’ять шляхів метаболізму ліпідів у печінці:
- окиснення жирних кислот до ацетил-КоА і далі до СО2 з утворенням АТФ;
- утворення кетонових тіл як транспортної форми ацетильних груп;
- біосинтез холестеролу і жовчних кислот;
- біосинтез ліпідної частини ліпопротеїнів плазми крові з жирних кислот;
- утворення комплексу жирних кислот з альбуміном сироватки крові, у складі якого жирні кислоти транспортуються до місця їх окиснювання в тканинах.
Основна маса гліцеролів ендогенного походження транспортується ліпопротеїнами дуже низької щільності, ефірів холестерину — ліпопротеїнами високої щільності (див. Ліпопротеїни). Основним місцем синтезу ліпідів є не лише печінка, а й клітини кишечнику. Продукти перетравлення ліпідів ресинтезуються у властиві для відповідного організму Л. Ресинтезований жир і частково продукти метаболізму потрапляють до лімфатичних капілярів і капілярів портальної вени (до 15%). Ліпіди транспортуються в інші органи і тканини в складі розчинних у воді ліпопротеїнових комплексів: зі стінки кишечнику — у вигляді хіломікронів, а з печінки — у вигляді ліпопротеїнів різної щільності. З чотирьох типів ліпопротеїнів у кишечнику утворюються два: хіломікрони і ліпопротеїни дуже низької щільності. З плазми крові всі ліпопротеїнові комплекси транспортуються до органів і тканин. В організмі немає органа, який би вибірково регулював метаболізм Л. Накопичення і використання Л. не залежить від рівня жирних кислот у крові; всі процеси здійснюються в печінці і спеціалізованій жировій тканині за участю нервової та гуморальної регуляції під контролем гормонів гіпофізу, надниркових і статевих залоз. Жирова тканина складається з високоспеціалізованих клітин, або адипоцитів. Вона міститься під шкірою, навколо кровоносних судин, у черевній порожнині. Середня маса жирової тканини молодого чоловіка з середньою масою тіла дорівнює масі м’язів і становить близько 20 кг. Жирова тканина рясно іннервована і пронизана кровоносними капілярами, здатна поглинати тригліцероли з крові й повертати у кров’яне русло жирні кислоти. Вона бере участь в активній взаємодії між печінкою, кістяковими м’язами і серцем. Ліпазна активність жирової тканини використовується для забезпечення енергетичних потреб організму. Встановлено ob-ген ожиріння та його генний продукт — лептин. Лептин утворюється у жировій тканині і може бути речовиною, яка бере участь у регулюванні величин депо жиру. Метаболізм фосфоліпідів — складний взаємозалежний процес, що характеризується великою кількістю попередників синтезу проміжних продуктів і наявністю альтернативних шляхів біосинтезу. Особливо інтенсивно ці процеси проходять у печінці, нирках, м’язовій тканині, менш інтенсивно — у тканинах головного мозку. Біосинтез холестеролу відбувається майже в усіх органах і тканинах. Особливо висока інтенсивність біосинтезу в надниркових залозах, нирках, сім’яниках, тонкій кишці та шкірі. Чільне місце в метаболізмі холестеролу посідає печінка, в якій здійснюється його біосинтез і подальше утворення жовчних кислот. За другорядним шляхом використання холестерол перетворюється на прогестерон, який є загальним попередником біосинтезу стероїдних гормонів.
Порушення ліпідного обміну супроводжуються стеатореєю, тобто появою ліпідів у калі. На порушення ліпідного обміну вказує зміна вмісту триацилгліцеролів, холестеролу та ліпопротеїдів у сироватці крові. Відомо п’ять типів гіперліпопротеїнемії, що характеризується підвищеним вмістом складних Л. у крові. Гіполіпопротеїнемія буває вродженою чи вторинною внаслідок порушення всмоктування жирів, їхнього прискореного розпаду в тканинах або через масивну крововтрату. Порушення перетравлення і всмоктування Л. можуть бути зумовлені: дефіцитом панкреатичної ліпази в підшлунковій залозі; дефіцитом жовчі в кишечнику при звуженні або закупорці жовчних протоків у фістулі жовчного міхура; зниженням метаболічної активності слизової оболонки кишечнику, де локалізовані ферменти ресинтезу триацилгліцеролів. Надлишкове надходження вуглеводів з їжею, яке не компенсується енерговитратами, може супроводжуватися надмірним накопиченням Л. Недостатнє надходження вуглеводів, енерговитрати, які не компенсуються вуглеводами, а також порушення метаболізму глюкози при цукровому діабеті супроводжується мобілізацією Л. і появою кетозу. Дефіцит холіну і донаторів метильних груп (метіоніну, вітамінів групи В) у харчуванні лімітує синтез фосфатидилхоліну, одного з найбільш розповсюджених фосфоліпідів. У цьому разі підсилюється синтез ацилгліцеролів, що може призвести до жирового переродження печінки з подальшим заміщенням гепатоцитів сполучною тканиною (див. Гепатоцит). До порушень ліпідного обміну належать надмірна маса тіла (див. Ожиріння), атеросклероз, коронарна хвороба серця та інсульти; прискорюється виникнення цукрового діабету. Причина артеріосклерозу — порушення в будь-якій ділянці метаболізму холестеролу: синтез, обмін, транспортування і виведення, формування ліпопротеїнів (особливо ліпопротеїнів низької щільності), їх катаболізм, рецепція ліпопротеїнів клітинами. У разі гіперхолестеринемії зменшують споживання жиру, надходження холестеролу (яйця, тваринний жир, субпродукти), збільшують частку ненасичених жирних кислот за рахунок вживання риб’ячого жиру або рослинної олії. β-Фітостерин з останньої утворює в кишках нерозчинні комплекси з холестеролом, внаслідок чого зменшується холестеринемія.
Перекисне окиснення ліпідів. (ПОЛ) молекулярним киснем характерне для ненасичених жирних кислот у складі ліпідів. ПОЛ — звичайний метаболічний процес, необхідний для здійснення процесів оновлення Л. мембран, синтезу метаболітів арахідонової кислоти, активації макрофагів, руйнування ксенобіотиків в організмі, знищення клітин, які переродилися, тощо. Утворення перекисних угруповань призводить до ушкодження біологічних мембран різного типу (ендоплазматичної мережі, мітохондріальних, ядерних тощо) і значно прискорюється при патологічних станах, хронічному стресі, дії малих доз іонізуючого випромінювання та жорсткого УФ-світла, променевій хворобі, канцерогенезі тощо. ПОЛ — вільнорадикальний процес, який здійснюється за ланцюговим механізмом. Його моделлю може служити процес згіркнення жирів — окиснення під дією квантів світла та кисню повітря триацилгліцеролів, які містять залишки ненасичених вищих жирних кислот. Продуктами ПОЛ є дієнові кон’югати, гідроперекиси, альдегідоспирти, окси- і кетокислоти, двоосновні карбонові кислоти з меншою кількістю вуглецевих атомів, епоксиди, полімерні сполуки та ін. Цей аутокаталітичний процес призводить до швидкого згіркнення жирів: з’являється неприємний різкий запах, гіркий смак, токсичність. Визначення кількості дієнових кон’югатів, малонового діальдегіду та інших продуктів, що утворилися, використовують для оцінки інтенсивності процесів ПОЛ як у зразках жирів, так і в біологічному матеріалі (Л. біомембран). У нормі процеси ПОЛ у тканинах контролюються системою антиоксидантів і корелюють із рівнем метаболічних процесів. Так, у тканинах з високою інтенсивністю метаболізму вміст перекисів Л. зазвичай вищий. Ініціаторами процесу ПОЛ можуть бути сполуки, здатні утворювати вільні радикали, кванти УФ-світла, іони металів змінної валентності (Fe, Cu, Mn, Co). Найбільшу активність утворення пероксидів мають мембрани, що містять електронотранспортні ланцюги. Комплекс Fe2+– аскорбінова кислота активує переокиснення ліпідів у всіх типах біологічних мембран, а комплекс Fe2+– НАДФ·Н2 активує переокиснення Л. у мембранах ендоплазматичної мережі, де розташована ферментна система переокиснювання Л. Отже, концентрація іонів Fe2+ є чинником, здатним регулювати процеси ПОЛ. Антиоксиданти (див. Антиоксиданти) ефективно гальмують процес ферментативного окиснення Л., якщо додавати їх на початку реакції і при розвитку процесу.
Тваринні жири та рослинні жирні олії одержують методами витоплювання та пресування. Суму Л. з біологічного матеріалу екстрагують органічними розчинниками, а потім фракціонують і виділяють індивідуальні Л. хроматографічними методами. Окремі групи речовин одержують у вигляді суміші однотипних сполук, які мають однакові голівки, але різну довжину і ступінь ненасиченості аліфатичних ланцюгів. Широко розповсюджені напівсинтетичні методи — переацетилювання природних Л. і перетворення одних класів Л. на інші за допомогою фосфоліпази. Чисті фосфоліпіди і сфінголіпіди для дослідження одержують повним хімічним синтезом. Цим же шляхом вивчають простагландини (див. Простагландини) та інші ейкозаноїди.
Біологічні функції ліпідів:
- основна форма запасання енергії;
- компоненти біологічних мембран;
- попередники важливих сполук (простагландинів, простациклінів, лейкотриєнів, тромбоксанів);
- виконують роль бар’єрів, які захищають органи і тканини від наслідків термічної, електричної та фізичної взаємодії;
- входять до складу оболонок, які захищають від інфекцій та надлишкової втрати або накопичення води;
- деякі з них є вітамінами і гормонами.
В організмі ссавців ліпіди є найважливішим енергетичним субстратом в окисних процесах, під час яких утворюється також ендогенна вода. Резервні Л. — це жири жирових депо; їх кількість і склад мінливі й залежать від режиму харчування та фізичного стану організму. Вміст і склад структурних Л. в організмі суворо постійні, генетично зумовлені і в нормі не залежать від харчування й функціонального стану. Крім того, жири підшкірної клітковини відіграють термозахисну роль, а також оберігають внутрішні органи і тканини від механічних ушкоджень. Ліпіди є найважливішими структурними компонентами клітинних мембран і субклітинних структур. Холестерол виконує в організмі важливі біологічні функції: утримання вологи і забезпечення необхідного тургору клітин, участь у процесах осмосу і дифузії, служить субстратом для утворення жовчних кислот, стероїдних і статевих гормонів, вітаміну D3 — холекальциферолу. Сфінголіпіди і фосфоліпіди необхідні для нормального функціонування нервової тканини.
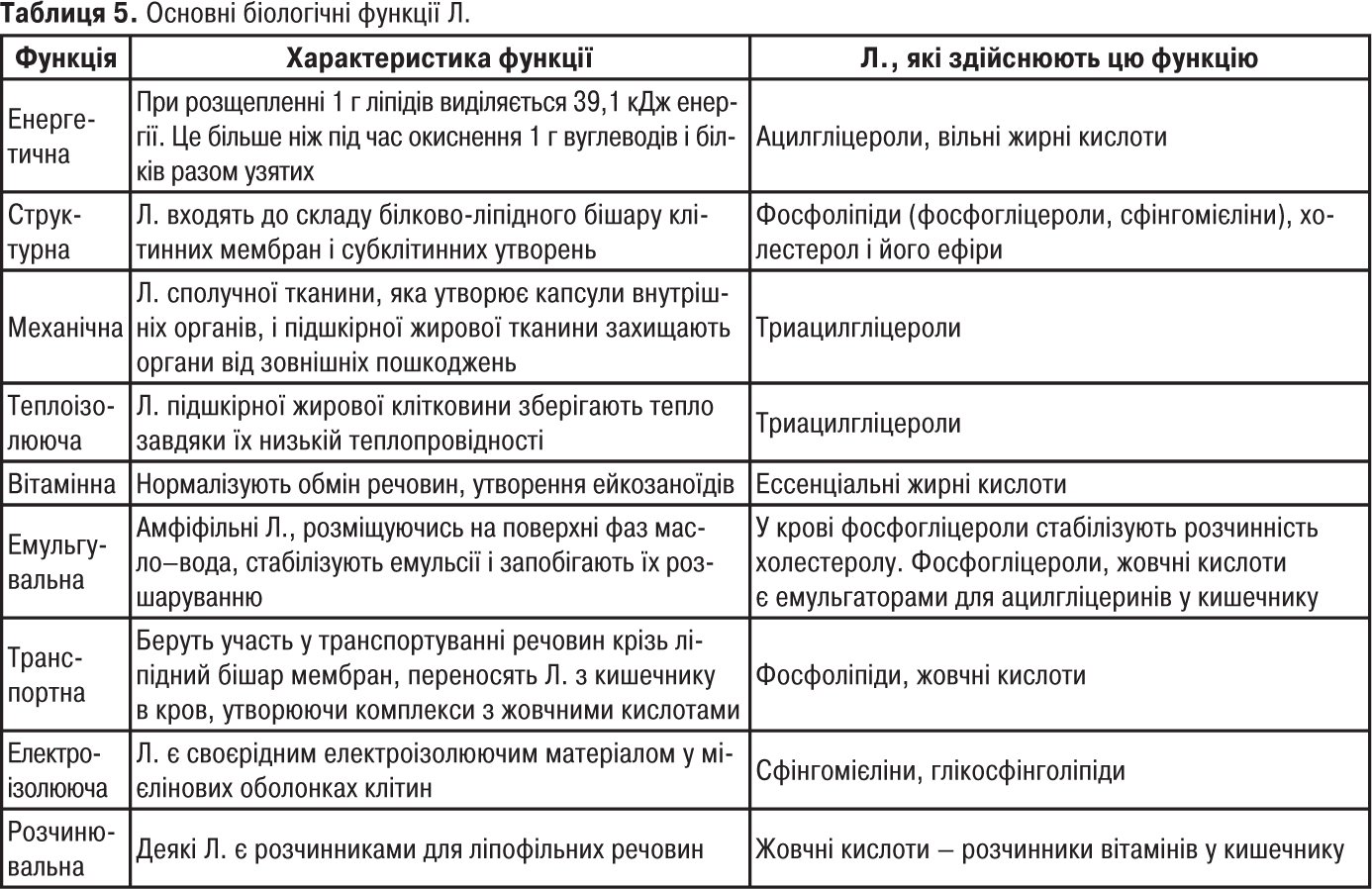
Незамінні жирні кислоти (вітамін F) служать джерелом утворення ейкозаноїдів (табл. 5).
Біологічну активність мають фосфоліпіди та інші сполуки ліпідної природи, такі як каротиноїди, похідні стеринів, вітаміни групи D, токофероли, хінони з бічним вуглецевим ланцюгом ізопреноїдної структури, зокрема вітаміни групи К, похідні бензохінону — убіхінон і пластохінон, стероїдні гормони. Методами модифікації ліпідного складу біологічних мембран визначені так звані ліпідозалежні ферменти, для функціонування яких необхідні Л. За допомогою цих ферментів здійснюється ліпід-білкова взаємодія в мембранах. Ліпіди також відіграють помітну роль у реалізації активності геному на стадії реплікації ДНК, впливають на взаємодію гормонів і токсинів з клітинними рецепторами.
Біохімічні дослідження ліпідів проводять головним чином у плазмі або сироватці крові, рідше — у калі (з метою діагностики) стеатореї та в сечі (при ліпурії). Визначення ліпідів у плазмі крові особливо важливе при захворюваннях, які супроводжуються підвищенням їх рівня в крові (гіперліпідемії). До них належать деякі захворювання печінки (гострі та хронічні гепатити, цироз тощо), цукровий діабет, атеросклероз, панкреатити, гіпертиреоз. Широко використовується визначення холестеролу і триацилгліцеролів у крові при фенотипуванні первинних і вторинних гіперліпопротеїнемій з метою діагностики та раціонального дієтичного і медикаментозного лікування. Зниження рівня ліпідів у крові (гіполіпідемія) спостерігається досить рідко: при тривалому голодуванні або різко обмеженому вживанні жирів та при гіпертиреозі. Дослідження ліпідів у крові проводять натще через 10–12 год після останнього вживання їжі.
БМЭ. — М., 1988. — Т. 14; Грубер-Швенк Г., Швенк М. Харчування: dtv-Atlas. — К., 2004; Кучеренко Н.Е., Васильев А.Н. Липиды. — К., 1985; Стопский В.С., Ключкин В.В., Андреев Н.В. Химия жиров и продуктов переработки жирового сырья. — М., 1992; Химическая энциклопедия. В 5 т. — М., 1990.
