АЛКАЛОЇДИ ХІННОЇ КОРИ — містять хінолінове кільце (див. Хінолін) та хінуклідинову систему, яка складається з двох конденсованих піперидинових циклів із чотирма спільними атомами карбону в положеннях 1, 2, 3, 4 та атомом нітрогену:
Хінолін Хінуклідин

Природним джерелом отримання А.х.к. є хінне дерево Cinchona Remijia (кора), основним представником якого є хінін. Іншими алкалоїдами є хінідин, цинхонін, цинхонідин і купреїн. Їх вміст у сухій хінній корі становить 2–15%. Хінна кора була відома в Європі вже в першій половині XVII ст. як протималярійний засіб, проте хінін виділено лише у 1814 р. харківським професором Ф.І. Гізе, а в 1820 р. — французькими фармацевтами Пелетьє і Кавенту. Хімічну будову хініну встановлено у 1907 р., а повний синтез здійснено у 1945 р. американськими вченими Вудвордом і Дерінгом.
Загальна формула А.х.к.:
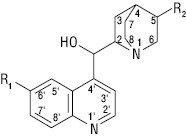
Відрізняються алкалоїди один від одного радикалами (таблиця).
Таблиця. Радикали й оптична ізомерія
| R1 | R2 | А.х.к. | |
| l-ізомер | d-ізомер | ||
| CH3O- H- CH3O- H- OH- |
CH2=CH- CH2=CH- CH3-CH2— CH3-CH2— CH2=CH- |
Хінін Цинхонідин Гідрохінін Гідроцинхонідин Купреїн |
Хінідин Цинхонін Гідрохінідин Гідроцинхонін – |
Хінін — двотретинна нітрогеновмісна основа, зумовлена наявністю двох атомів нітрогену (у хіноліновій і хінуклідиновій системах). Більш сильні основні властивості виявляє нітроген хінуклідинового циклу. Як двокислотна основа хінін утворює два типи солей — основні та нейтральні. Солі, які містять два еквіваленти кислоти, в розчинах піддаються гідролізу і мають кислу реакцію середовища.
Для застосування в медичній практиці хінін добувають з кори хінного дерева. Кору подрібнюють і розмішують із сумішшю Са(ОН)2 та NaOH. Алкалоїди переходять в основи, їх екстрагують при 60–65 °С органічними розчинниками. Екстракт промивають розбавленою H2SO4, при цьому випадає хініну сульфат у вигляді осаду, який очищують перекристалізацією. Інші алкалоїди розділяють за допомогою іонообмінної хроматографії. З сульфату одержують шляхом обміну з солями барію різні інші солі хініну. У фармакотерапії застосовують найчастіше сульфат (див. Хініну сульфат), хлорид (див. Хініну гідрохлорид) і дихлорид хініну.
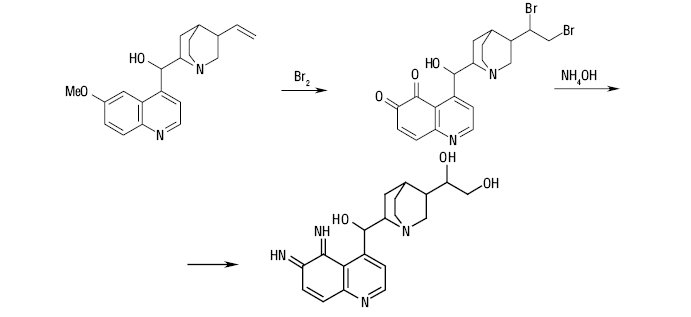
За фізичними властивостями солі хініну — безбарвні кристалічні речовини без запаху, дуже гіркі на смак. Під дією світла поступово жовтіють. У медичній практиці застосовують у вигляді лівообертаючих ізомерів. Солі хініну розрізняють за розчинністю у воді: дигідрохлорид — дуже легкорозчинний, гідрохлорид — розчинний, а сульфат — малорозчинний. Загальною груповою реакцією на алкалоїди групи хініну є талейохінна проба: до розчину солі хініну додають декілька крапель бромної води та розчин аміаку — з’являється смарагдово-зелене забарвлення:
У деяких джерелах літератури структуру талейохініну наведено інакше:
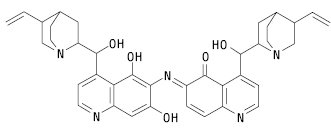
А.х.к., які не мають замісників у 6´-положенні, цю реакцію не дають. Солі хініну сульфату у воді, а інші солі в оксигеновмісних кислотах мають блакитну флюоресценцію. Цього випробування не зазнають цинхонін та інші А.х.к., які не мають метоксигрупи в 6´-положенні. Флуоресценція розчинів хініну як двоосновної основи залежить від рН середовища. У кислому середовищі хінін має блакитну флуоресценцію, а в лужному середовищі (рН ≈9) — фіолетову. Розчини сполук окиснення хініну мають жовто-зелену флуоресценцію. Для ідентифікації солей хініну використовують осадові (загальноалкалоїдні) реактиви на органічні нітрогеновмісні основи (пікринова кислота, ртуті дихлорид, танін, кислота фосфорновольфрамова та ін.). У токсикологічному аналізі використовують мікрокристалоскопічну реакцію утворення герепатиту. Реакцію проводять у спиртовому середовищі дією спиртового розчину йоду за наявності сульфатної кислоти — утворюються характерні (у вигляді листочків) зелені кристали складу:
[C20H24O2N2]4 ⋅ (H2SO4)2 ⋅ (HI)2 ⋅ I4 ⋅ 6H2O.
Кількісне визначення солей хініну проводять методами кислотно-основного титрування у неводному середовищі, у змішаних розчинниках (вода-хлороформ-етанол), гравіметрії, броматометрії та ін.
Використовують хінін у фармакотерапії завдяки протималярійній дії, яка може бути пов’язана зі здатністю його концентруватися в лізосомах клітин плазмодії; при цьому підвищується pH внутрішньоклітинних органел, що спричиняє порушення транспорту макромолекул і активність фосфоліпази. Можливо, блокується синтез нуклеїнових кислот у клітинах плазмодію. Хінін також має шизонтоцидну дію. Його здатність накопичуватися в уражених еритроцитах пояснює його токсичну дію проти еритроцитарних форм усіх 4 видів плазмодіїв, що викликають малярію, зокрема штами Plasmodium falciparum, резистентні до хлорохіну. Хінін також має гаметоцидну дію відносно Plasmodiumvivax і Plasmodium malariae. Хінін зумовлює антиміотонічний ефект — подовжує рефрактерний період скелетних м’язів шляхом прямого впливу на м’язове волокно і розподілення кальцію всередині волокна, таким чином послаблюючи відповідь на м’язову стимуляцію. Він також зменшує збудливість закінчень рухового нерва і знижує відповідь на повторну нервову стимуляцію та на ацетилхолін. Хінін пригнічує теплорегулюючі центри і знижує температуру тіла при гарячкових станах. Посилює скорочення м’язів матки. При застосуванні швидко й майже повністю всмоктується у ШКТ, біодоступність ≈80%. Тmax після вживання — 3–5 г. Поєднання з білками плазми крові — 70–90%. За час нападів малярії концентрація хініну в плазмі крові значно вища, ніж в еритроцитах. Проходить через гематоенцефалічний бар’єр (відношення вмісту в спинномозковій рідині до рівня у плазмі крові становить ≈7%). Проходить через плаценту і проникає в грудне молоко; Сmax у материнському молоці досягається протягом ≈90 хв після вживання. Метаболізується в печінці (>80%), метаболіти мають меншу активність, ніж хінін. Виділяється нирками (більш інтенсивно при кислій реакції сечі). Т½ у хворих дорослих становить 16–18 год (у здорових людей — ≈11 год, у дітей — 12 год). Практично не видаляється з організму при діалізі. ЛП хініну залишаються препаратами вибору для лікування у разі тяжкої тропічної малярії, спричиненої штамами, стійкими до хлорохіну, піриметамін/сульфадоксину, мефлохіну або полірезистентними штамами Plasmodium falciparum. Іноді застосовують у поєднанні з піриметамінсульфадоксином. Можливе застосування хініну при слабкості пологової діяльності, гіпотонії матки в ранній післяпологовий період (у складі комбінованої терапії). У зв’язку зі здатністю знижувати збудливість серцевого м’яза і подовжувати рефрактерність можливе застосування хініну для лікування та запобігання екстрасистоліям, зазвичай у поєднанні з препаратами наперстянки. Хініну сульфат додається як смакова добавка у харчові напої, такі як тоніки і джин-тоніки.
Беликов В.Г. Фармацевтическая химия. — Пятигорск, 1996; ДФУ. — Х., 2001; Машковский М.Д. Лекарственные средства. — М., 2012; Туркевич М.М., Владзімірська О.В., Лесик Р.Б. Фармацевтична хімія. — Вінниця, 2003; Фармацевтическая химия / Под ред. А.П. Арзамасцев. — ГЭОТАР-Медиа. — М., 2006; Химическая энциклопедия: В 5 т. / Под ред. И.Л. Кнунянц и др. — М., 1988.
