Окисно-відновні реакції — реакції, які супроводжуються переходом електронів від одних атомів, молекул або іонів до інших при зміні ступеня окиснення елементів. Речовину, що містить елемент, який віддає електрони, називають відновником. Процес віддачі електронів, при якому ступінь окиснення елемента зростає, називають окисненням. Речовину, що містить елемент, який приєднує електрони, називають окисником. Процес приєднання електронів називають відновленням. При відновленні ступінь окиснення елемента знижується. Ступінь окиснення елемента — це той електричний заряд атома цього елемента у сполуці, який розраховується, виходячи з припущення, що сполука складається з іонів. Або це той умовний заряд, який мав би атом елемента у сполуці при повному переході електронних пар, які утворюють зв’язок, до більш електронегативних атомів. Процеси окиснення та відновлення проходять одночасно і загальне число електронів, відданих відновником, дорівнює числу електронів, прийнятих окисником. У загальному вигляді О.-в.р. можна записати так: Am + Bp → Am-n + Bp+n, де: відновник: Am — nē ↔ Am-n — процес окиснення відновника; окисник: Вр + nē ↔ Bp+n — процес відновлення окисника.
Здатність атомів елементів утримувати власні електрони і приєднувати нові характеризується значенням відносної електронегативності атома (χ). Елементи-окисники мають велике значення χ (3,5–4,0), елементи-відновники — χ≤1, елементи, які мають окисно-відновну двоїстість, значення χ≈2. Таким чином, оскільки окисно-відновна активність простих речовин залежить від електронної конфігурації їх атомів, вона змінюється періодично від відновної у лужних металів до окисної у галогенів. У головних підгрупах окисна здатність елементів зменшується. Отже, найбільш сильним окисником є F, а відновником — Fr. У хімічних сполуках елементи мають різний ступінь окиснення. Сполуки, в яких елемент знаходиться у вищому ступені окислення, виявляють лише окисні властивості (віддані всі валентні електрони). Сполуки, в яких елемент знаходиться у нижчому ступені окиснення, виявляють лише відновні властивості (немає вільних орбіталей валентного рівня). Сполуки, в яких елемент знаходиться у проміжному ступені окиснення, виявляють окисно-відновну двоїстість. У металів значення χ незначне, тому всі метали у вільному стані виявляють лише відновні властивості. А для неметалів у вільному стані характерна окисно-відновна двоїстість (крім F), оскільки вони знаходяться на проміжному ступені окиснення, і значення χ у них досить велике. На перебіг О.-в.р. впливають: рН середовища, температура, концентрації речовин, наявність каталізатора, співвідношення сили окисника і відновника, а для реакцій, що проходять у газовій фазі, — тиск. Розрізняють три типи О.-в.р. Міжмолекулярними називають реакції, в яких елементи, що змінюють ступені окиснення, знаходяться у складі різних молекул:
2KBr–1 + Cl02 → Br02 + 2KCl–1.
Відновник Окисник
До цього типу належать і такі реакції, в яких у відновника та окисника атоми, які змінюють ступінь окиснення, є атоми одного і того ж елемента в різних ступенях окиснення:
–2 +4 0
2H2S + H2SO3 → 3S + 3H2O.
Відновник Окисник
У таких випадках унаслідок результатів реакції утворюється сполука цього елемента зі ступенем його окиснення, проміжним між відновником та окисником. Внутрішньомолекулярними називають реакції, в яких ступінь окиснення змінюють два елементи, які входять до складу однієї молекули, але це або різні атоми, або атоми одного елемента з різними ступенями окиснення:
–3 +6 0 +3
(NH4)2Cr2O7→N2+Cr2O3+4H2O
(N-3 — відновник, Cr+6 — окисник).
–3 +3 0
NH4NO2→N2+2H2O
(N-3 — відновник, N+3 — окисник).
Реакції диспропорціювання (дисмутації) — реакції, внаслідок яких одночасно підвищується і знижується ступінь окиснення атомів одного елемента. У цьому разі він одночасно виконує роль і відновника, і окисника.
2Н2О–12 → 2Н2О–2 + О02.
Для складання рівнянь О.-в.р. необхідно знати емпіричні формули вихідних речовин і продуктів реакції, які визначають експериментально чи на основі властивостей елементів. При написанні таких рівнянь слід дотримуватися законів збереження маси речовини та збереження заряду. У рівняннях О.-в.р. прийнято спочатку записувати відновник, далі окисник і потім речовину, яка зумовлює середовище. Відповідно у продуктах реакції спочатку записують продукт окиснення відновника, далі — продукт відновлення окисника, а потім інші продукти реакції. Для визначення коефіцієнтів у рівняннях О.-в.р. використовують два методи. Метод електронного балансу: універсальний, який застосовується для всіх реакцій в усіх агрегатних станах. Він ґрунтується на обліку зміни ступенів окиснення елементів вихідних речовин і продуктів реакції. Користуючись цим методом, спочатку записують схему реакції, напр.:
–1 –1 0 –2
KІ+ H2О2 → І2 + KOH,
а потім розраховують ступені окиснення всіх елементів, знаходять окисник та відновник і записують над ними ступені окиснення атомів, що їх змінили. Записують електронні схеми, які відображають процеси відновлення та окиснення:
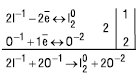
Оскільки кількість електронів, відданих відновником, має дорівнювати кількості електронів, приєднаних окисником, знаходять найпростіше співвідношення кількості відновника та окисника, що задовольняє цю умову (у цьому разі 1 — для відновника і 2 — для окисника). Їх записують праворуч від електронних схем — це множники, на які слід помножити кожну напівреакцію, щоб зрівняти числа електронів у О.-в.р. Після цього розставляють ці коефіцієнти у рівняння реакції:
2KІ + H2О2 → І2 + 2KOH.
Потім, якщо це необхідно, знаходять коефіцієнти для інших речовин: спочатку зрівнюють усі катіони, крім Н+, далі аніони, потім кількість Н+. Перевіряють правильність, зрівнюючи кількість атомів Оксигену ліворуч і праворуч у рівнянні. Якщо кількість елементів, які змінюють ступінь окиснення, більша двох, то розраховують загальну кількість електронів, відданих відновниками і приєднаних окисниками:
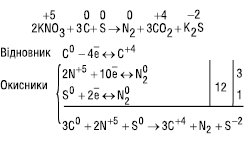
Іонно-електронний метод (метод напівреакцій) застосовується для визначення коефіцієнтів у рівняннях О.-в.р., які перебігають у розчинах або розплавах. Згідно з цим методом враховують взаємодію молекул та іонів, які реально існують у середовищі. Процеси окиснення та відновлення записують у вигляді іонних напівреакцій, враховуючи дисоціацію речовин. За цим методом спочатку записують схему реакції, знаходять окисник та відновник і записують над атомами їх покажчики окиснення, що змінили ступені:
H2S–2 + K2Cr+62 O7 + H2SO4 → S0 + Cr+32 (SO4)3 +…
Складають іонну схему реакції:
H2S + Cr2O2-7 + Н+ → S + Cr3+ + Н2О.
Потім складають рівняння напівреакцій. У кислому середовищі надлишкові атоми Оксигену зв’язують Н+ — на кожний надлишковий атом Оксигену додають два Н+, а в другу частину рівняння — відповідну кількість Н2О. Так само, як і в методі електронного балансу, знаходять коефіцієнти в О.-в.р.:
H2S — 2ē 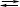 S + 2H+ 3
S + 2H+ 3
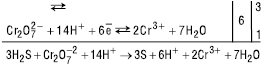
Скорочують однакові іони та молекули праворуч і ліворуч у повному іонному рівнянні О.-в.р.
Скорочене іонне рівняння реакції має вигляд:
3H2S+ Cr2O2-7 +8H+ → 3S+2Cr3++7 Н2О.
На його основі записують молекулярне рівняння, підбираючи для катіонів аніони, які знаходяться у розчині, і навпаки:
3H2S + К2Cr2O7 + 4H2SО4 → 3S + Cr2(SO4)3 + К2SO4 + 7 Н2О.
Для О.-в.р., які відбуваються у лужному чи нейтральному середовищі, надлишкові атоми Оксигену зв’язують Н2О — на кожний надлишковий атом Оксигену додають молекулу Н2О, а у протилежний бік рівняння — вдвічі більшу кількість ОН–:
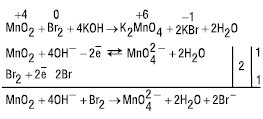
Кількісною характеристикою окисної чи відновної властивості різних речовин є окисно-відновний потенціал, який характеризує прагнення цього окисника приєднувати електрони, а відновника — їх віддавати. Користуючись величинами стандартних окисно-відновних потенціалів (Е0), значення яких наведені в довідкових таблицях, можна визначити напрямок О.-в.р. Головною умовою їх перебігу є додатне значення електрорушійної сили (ЕРС) О.-в.р. Для її обчислення від величини Е0 окисника віднімають величину Е0 відновника:
ЕРС = Е0окисн. — Е0відновн.
Типовими О.-в.р. є реакції клітинного дихання, фотосинтезу, реакції горіння та інші важливі природні та технічні процеси.
Краткая химическая энциклопедия. — М., 1988; Кудрявцев А.А. Составление химических уравнений. — М., 1962; Левитин Е.Я., Бризицкая А.Н., Клюева Р.И. Общая и неорганическая химия. — Х., 2002.
