ГРАВІМЕТРІЯ (ваговий аналіз; лат. gravimetria < лат. gravis — важкий + грец. metron — мірка) — метод кількісного аналізу, що базується на точному вимірюванні маси досліджуваного компонента аналізованої суміші чи досліджуваної речовини, виділеної у хімічно чистому вигляді або у вигляді хімічної сполуки з точно відомим складом.
Розрізняють гравіметричні методи осадження, відгонки та виділення.
У методах осадження досліджуваний компонент кількісно осаджують хімічними способами у вигляді малорозчинної сполуки сталого складу (осаджена форма). Утворений осад піддають аналітичній обробці, тобто відокремлюють фільтруванням, декантацією або іншим способом, промивають від залишків сорбованих осадом компонентів, іноді переосаджують. Потім підсушують або прожарюють до утворення стійкої сполуки зі сталим складом (гравіметрична чи вагова форма), масу якої вимірюють на аналітичних терезах. Осаджена і гравіметрична форма можуть збігатися або відрізнятись. Напр. при визначенні Ва2+ осаджена і гравіметрична форми — BaSO4; при визначенні Са2+ осаджена форма — СаС2О4, гравіметрична форма — СаО або СаСО3.
Розрахунки вмісту w (% за масою) досліджуваного компонента здійснюють за формулою:
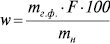 ,
,
де mг.ф. — маса гравіметричної форми, г; mн — маса наважки, г; F — гравіметричний фактор, який дорівнює співв1дношенню мол. м. сполуки, що визначається (М1), і мол. м. гравіметричної форми (М2):
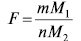 ,
,
де m і n — стехіометричні коефіцієнти в рівнянні хімічного перетворення досліджуваного компонента в його гравіметричну форму.
Гравіметричні методи осадження дозволяють кількісно визначити практично всі найбільш важливі катіони та аніони неорганічної природи, а також низку органічних сполук, у т.ч. і лікарських, напр. лактозу в молочних продуктах, саліцилати в лікарських речовинах, нікотин в отрутохімікатах, холестерин у сироватці крові.
У методах відгонки досліджуваний компонент відокремлюють з аналізованої проби і кількісно відганяють у вигляді леткої сполуки. Метод відгонки називають прямим, якщо масу газоподібної речовини вимірюють безпосередньо або за приростом маси поглинальної трубки. Напр. визначення вмісту СО2 в СаСО3 здійснюють за збільшенням маси попередньо зваженої на анaлітичних терезах поглинальної трубки з NaOH. Метод відгонки називають непрямим, якщо масу леткої речовини визначають за різницею мас до і після відгонки (напр. вміст вологи у препаратах, кристалізаційної води, іноді — карбонатів, сульфідів, сульфітів після обробки проб кислотою). Розрахунки вмісту w (% за масою) досліджуваного компонента здійснюють за формулами:
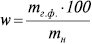
(пряма відгонка),
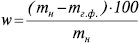
(непряма відгонка).
У методах виділення досліджувану речовину кількісно виділяють у вільному стані і зважують на аналітичних терезах. Методи використовують для встановлення доброякісності ЛП. За допомогою цих методів встановлюють загальну золу; золу, не розчинну в хлоридній кислоті, а також сульфатну золу. Розрахунки вмісту w,% здійснюють за формулою
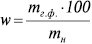 .
.
Розрізняють також електрогравіметрію. За цим методом осаджену форму виділяють на катоді (напр. Cu0) або на аноді (напр. Pb у вигляді PbO2) в результаті електролізу із зовнішнім джерелом електроструму або внутрішнім електролізом у гальванічній комірці. Вміст досліджуваного компонента визначають за приростом маси електрода.
За методом термогравіметрії визначають термічно нестійкі речовини. Масу встановлюють із використанням термотерезів. Визначення кількох компонентів досліджуваної суміші проводять за термогравіметричними кривими.
Недоліком гравіметричних методів аналізу є їх тривалість і трудоємність, але серед хімічних методів аналізу саме ці методи найточніші: відносна помилка становить до ±0,1% (іноді до ±0,01%). Методи не потребують зразків порівняння, тому їх застосовують для перевірки інших методів аналізу, для арбітражного аналізу, а також для атестації стандартних зразків.
Аналитическая химия / В.В. Болотов, А.Н. Гайдукевич, Е.Н. Свечникова и др. — Х., 2000; Крешков А.П. Основы аналитической химии. — М., 1976. — Т. 2; Посыпайко В.И., Козырева Н.А., Логачева Ю.П. Химические методы анализа. — М., 1989.
