Алкалоїди (лат. alkali — луг + oides — подібний, тобто подібні до лугу) –велика група вторинних рослинних речовин, які містять один чи більше атомів азоту, частіше у складі гетероциклічного кільця, мають лужні властивості, більшість з них чинить виражену фармакологічну дію на організм людини і тварин. Алкалоїди не є гомологічною групою речовин і розрізняються за хімічними, біохімічними і фармакологічними властивостями. Крім С, Н, О і N, молекули А. містять атоми S, рідше Cl чи Br.
Алкалоїди зазвичай надають назви рослин, з яких їх виділяють.
Назва алкалоїдів може бути:
- за родовою назвою рослини (атропін — Atropa);
- за видовою назвою рослини (кокаїн — Erytroxylon coca);
- за фізіологічною активністю (морфін — від імені бога сну Морфея);
- за назвою рослинної сировини (ерготамін — від назви ріжок (рос. назва: спорынья) ergot);
- або називають іменем першовідкривача (Пелетьє — пелетьєрин).
Іноді до назви алкалоїдів додають префікс чи суфікс, щоб позначити інший А. з цього ж рослинного джерела, проте відповідно до хімічної номенклатури назва алкалоїдів має закінчуватися на суфікс -ін.
Найбільш прийнятна класифікація алкалоїдів, що базується на будові вуглецево-азотного скелета молекули, напр.: ізохінолінові алкалоїди, тропанові, індольні, хінолінові, пуринові, імідазольні, піридинові, піперидинові, хінолінові, піролідинові.
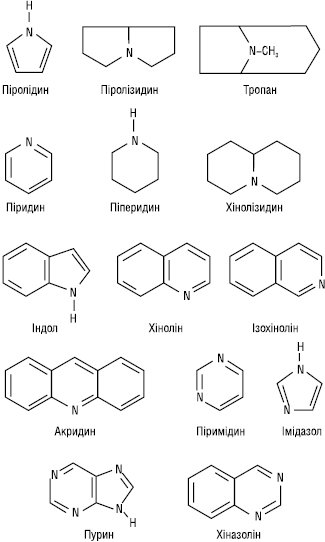
Класифікують також за філогенетичними ознаками, поєднуючи в одну групу всі сполуки, виділені з рослин однієї родини чи роду, напр.: А. аконіту, А. дурману, А. іпекакуани, А. родини Макових.
За біогенетичними попередниками (прекурсорами) можна групувати А., розрізняючи групи А., у біосинтезі яких беруть участь амінокислоти орнітин, лізин, пролін, фенілаланін, триптофан, антранілова кислота і гістидин. З точки зору біосинтезу А. розподіляють на 3 групи: А., або справжні А., — мають гетероцикли і біосинтетично походять з А. амінокислот або з кислот нікотинової чи антранілової; протоалкалоїди (біогенні аміни) — містять азот поза циклом, але утворюються з амінокислот; псевдоалкалоїди (ізопреноїдні А.) — утворюються без участі амінокислоти, але за участю мевалонової кислоти і об’єднуються в групу незалежно від наявності гетероциклу, тобто вони мають терпеноїдне походження. Біохімічна класифікація А. не завжди дозволяє однозначно віднести той чи інший А., особливо складної структури, до певної групи. Можна системазувати А. за фармакологічним принципом, згрупувавши речовини з однотипною активністю. Напр., А. з протикашльовою дією — кодеїн, глауцин та ін.; А., що чинять спазмолітичний ефект — папаверин, атропін, платифілін та ін.
Зазвичай рослини містять суміш декількох, іноді до 15 або 20 А., які близькі за своєю будовою, напр. мак снодійний, хінне дерево. Однак деякі рослини містять тільки один А., напр. рицинін у рицині. Багато А., особливо складної будови, специфічні для певних родів і навіть родин, що широко використовуються у систематиці (хемотаксономія). Часто А. містяться в рослині у вигляді солей органічних та неорганічних кислот. Локалізацію А. виявляють переважно у певних частинах (органах) рослин, напр. у хінному дереві — кора, в аконіті — бульби, у кокаїновому кущі — листя, у болиголова — плоди, у фізостигмі — насіння. Вміст А. у тканинах зазвичай становить десяті або соті частки відсотка і рідко доходить до 10–15% (кора хінного дерева, лист тютюну). Значний вплив на накопичення А. у рослинах має географічне розповсюдження та різні фактори: температура повітря і ґрунту, кількість опадів, тривалість та інтенсивність сонячного дня, затемнення, висота над рівнем моря тощо, а також вплив людини у разі культивування та акліматизації.
Алкалоїди, які виявляють у тварин, не завжди синтезуються самим організмом, іноді їх походження пов’язане з характером їжі. Так, бобри, вживаючи в їжу кореневища латаття жовтого (рос. назва: кувшинка желтая), накопичують А. касторамін, дуже близький до А. нуфаридину.
Розчинність, екстракція та розділення А. залежать від форми, в якій вони знаходяться у рослинній сировині: А. у рослинах містяться у формі А.-основ, А.-солей і А.-N-оксидів. А.-основи розчинні в органічних розчинниках (спирті, ефірі, хлороформі, бензолі тощо) і, як правило, нерозчинні або малорозчинні у воді. Виняток: кофеїн, ефедрин, кодеїн, які розчинні у воді. Солі А. — білі кристалічні речовини, розчинні у воді й не розчинні в органічних розчинниках (крім спирту). Розчинність у воді різна; напр. для хініну сульфату — у співвідношенні 1:1000, а для хініну гідрохлориду — усього 1:1. Деякі солі А. (напр. папаверину гідрохлорид) розчинні у хлороформі. Більшість кисневмісних А. — тверді кристалічні сполуки, безбарвні або ледь забарвлені (як виняток — берберин жовтого кольору), гіркі на смак. А., які не містять кисню (напр. коніїн з болиголову, нікотин, пахікарпін) є рідинами, що переганяються з водяною парою, проте солі цих А. — тверді кристалічні сполуки. А. оптично активні, які обертають площину поляризованого променя ліворуч, мають більшу фармакологічну активність. Деякі А. в УФ-світлі мають характерну флуоресценцію. А. — досить слабкі основи. Константи дисоціації відомих А. коливаються у значних межах, а їх солі мають різний ступінь стійкості. А. з дуже малим ступенем дисоціації не утворюють солей (кофеїн, колхіцин). До найбільш сильних основ відносять кодеїн (К = 9·10–7), до найбільш слабких — кофеїн (К = 4,1·10–14). А. у водних або водно-спиртових розчинах виявляють лужну реакцію. Зазвичай рН водно-спиртових розчинів А. не перевищує 8–8,5. А. з кислотами утворюють солі, причому один азот молекули приєднує один еквівалент одноосновної кислоти. За другим азотом приєднання проходить важче, такі А. зазвичай приєднують також один еквівалент одноосновної кислоти (стрихнін). Луги й розчин аміаку, а іноді карбонати і оксид магнію розкладають солі А., витісняючи вільні основи. А., які містять фенольний гідроксил, утворюють з лугами феноляти. Так, морфін випадає в осад під дією лугів, а потім розчиняється в їх надлишку, що дає можливість визначити його серед інших А. А., що є складними ефірами (атропін, кокаїн), під дією лугів омилюються.
Найчастіше використовують такі методи виділення: екстракція А. у вигляді солей; екстракція А. у вигляді основ. За першим методом А. екстрагують хлороформом з рослинної сировини, попередньо змоченої лужними агентами (розчином аміаку чи карбонату натрію). За другим методом з рослинної сировини виділяють А. водним розчином кислоти чи спиртом (етанолом чи метанолом). Рідкі й леткі А. (нікотин і коніїн) одержують методом перегонки з парою.
На сьогодні у практичній медицині використовують >90 А., які застосовують у чистому вигляді та у вигляді галенових та новогаленових препаратів, що одержують з А. сировини, входять до складу багатьох комплексних препаратів.
Алкалоїди мають низку суттєвих негативних властивостей: при застосуванні деяких А. виникає залежність; багато з них є сильнодіючими отрутами, здатними призвести до летального наслідку.
Заготівлю, сушіння, переробку і зберігання сировини, яка містить А., проводять з урахуванням токсичності.
Гудвин Т., Мерсер Э. Введение в биохимию растений. В 2 т. — М., 1986; Орехов А.П. Химия алкалоидов. — М., 1955; Химическая энциклопедия / Гл. ред. И.Л. Кнунянц. — М., 1988. — Т. 1; Юнусов М.С. Алкалоиды. — Ташкент, 1981.
