Етери (грец. aethеr — ефір, небо, повітря) (прості ефіри) — похідні спиртів, енолів та фенолів (загальна формула R–O–R’). Якщо радикали однакові, то Етери — симетричні, якщо різні — несиметричні або змішані. Залежно від природи радикалів розрізняють діалкілові, діарилові, дициклоалкілові, арилалкілові, алкілвінілові та ін. Е. До Е. належать також гліми, карбітоли, целозольви та деякі гетероциклічні сполуки (1,4-діоксан, оксиран, оксолан, тетрагідрофуран тощо).
Назви етерів утворюють від назв вуглеводневих радикалів шляхом додавання суфікса -овий та слова «ефір», напр. СН3–О–СН3 — диметиловий ефір, СН3–О–С2Н5 — метилетиловий ефір. Е. розглядають як алкокси-, циклоалкокси-, арилоксипохідні вуглеводнів, у цьому випадку складніший радикал вважається родоначальною структурою: CH3-О-СН2–СН3 — метоксиетан, С2Н5О–С3Н7 — етоксипропан, С6Н5–ОСН3 — метоксибензол. Деякі етери мають тривіальні назви: С6Н5–ОСН3 — анізол, С6Н5О–С2Н5 — фенетол, 2-СН3ОС6Н4ОН — гваякол. Диметиловий та метилетиловий ефіри за звичайних умов є газами. Всі інші Е. — безбарвні рідини або кристалічні речовини з приємним або характерним «ефірним» запахом, поганорозчинні у воді, добре — в органічних розчинниках (таблиця).
Таблиця. Властивості етерів
| Формула | Назва | Ткип, оС | Тпл, оС |
| СН3ОСН3 | Диметиловий ефір (метоксиметан) | -23.7 | -138,5 |
| СН3ОС2Н5 | Метилетиловий ефір (метоксіетан) | 8 | – |
| С2Н5ОС2Н5 | Діетиловий ефір (етоксіетан) | 34,6 | -116,3 |
| С2Н5ОСН=СН2 | Метилвініловий ефір (етоксіетилен) | 36 | – |
| С3Н7ОС3Н7 | Дипропіловий ефір (пропоксипропан) | 91 | -122 |
| С6Н5ОСН3 | Метоксибензол (анізол) | 155 | -37 |
| С6Н5ОС2Н5 | Етоксибензол (фенетол) | 172 | -33 |
| С6Н5ОС6Н5 | Дифеніловий ефір (феноксибензол) | 259 | 27,5 |
Етери є досить інертними речовинами. Розведені мінеральні кислоти, водні розчини лугів та лужні метали з ними не взаємодіють. Реакційна здатність вінілових та арилових ефірів зумовлена вуглеводневими радикалами. Через неподілені пари електронів на атомі оксигену Е. виявляють слабкі основні властивості і з концентрованими мінеральними кислотами утворюють нестійкі оксонієві солі:
[RR’–OH]+Cl–,
а з кислотами Льюїса — ефірати (RR’OBF3). Діалкілові та алкіларилові ефіри розкладаються під дією НІ до галогеналкану і відповідного спирту або фенолу:
СН3ОСН3 + НІ → СН3ОН + СН3І.
Діарилові ефіри стійкі до дії концентрованої йодоводневої кислоти. Розщеплення метил- та етилалкілових ефірів використовують для кількісного визначення метокси- та етоксигруп (метод Цейзеля). Концентрована H2SO4 перетворює Е. на складні ефіри сірчаної кислоти, а вінілові ефіри в кислому середовищі гідролізуються до альдегідів або кетонів і спиртів:
![]()
Вінілові ефіри здатні полімеризуватися, що використовується у синтезі ВМС. При дії алкілнатрію або алкіллітію на Е. відбувається β-елімінування з утворенням алкенів:
CH3CH2OCH2CH3 + RNa 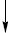 CH2=CH2 + C2H5ONa + RH.
CH2=CH2 + C2H5ONa + RH.
Арилалкілові ефіри під дією H2SO4, AlCl3 ізомеризуються в орто— та пара-алкілзаміщені феноли, а алілфенілові ефіри — в орто— та пара-алілфеноли. При тривалому стоянні Е. окиснюються киснем повітря з утворенням вибухонебезпечних гідропероксидів R–O–OH і пероксидів R–O–O–R. Тому перед використанням простих ефірів необхідно робити пробу з розчином KI. Наявність пероксидів підтверджує буро-коричневий колір розчину. Для руйнування пероксидів Е. обробляють NaOH або відновниками Na2SO3, FeSO4 та ін. Для одержання симетричних ефірів використовують реакцію міжмолекулярної дегідратації спиртів у присутності концентрованої H2SO4 або інших водовідбираючих речовин. Важливим методом синтезу симетричних і несиметричних ефірів є реакція алкоголятів і фенолятів з алкілгалогенідами (реакція Вільямсона). Для синтезу арилалкілових ефірів замість арилгалогенідів можна застосовувати діалкілсульфати:
C6H5ONa + (CH3)SO4 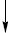 C6H5OCH3 + CH3OSO3Na.
C6H5OCH3 + CH3OSO3Na.
Етери також утворюються за реакцією приєднання спиртів або фенолів до олефінів. При нагріванні спиртів з ацетиленом одержують алкілвінілові ефіри:
HC=—CH + HOCH2CH3 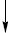 CH2=CH–O–C2H5.
CH2=CH–O–C2H5.
Взаємодія ацетилену з діазометаном призводить до утворення алкіл- та арилметилових ефірів.
Діетиловий ефір застосовують для виготовлення настоїв, екстрактів, деяких лікарських форм для зовнішнього застосування, обмежено — в хірургічній практиці для наркозу. Його суміш з етанолом у пропорції 1 : 3 під назвою крапель Гофмана використовують при запамороченні. Бутилвініловий ефір є вихідним продуктом синтезу полівінілбутилового ефіру, який застосовують при фурункулах, трофічних виразках, опіках, обмороженнях (бальзам М.Ф. Шостаковського або вінілін). До арилалкілових ефірів можна віднести і димедрол, який застосовують як антигістамінний препарат. Етери — розчинники жирів, лаків та інших органічних сполук. Використовуються у виробництві ароматичних речовин, барвників.
Химическая энциклопедия. В 5 т. — М., 1990. — Т. 5; Черных В.П., Зименковский Б.С., Гриценко И.С. Органическая химия / Под общ. ред. В.П. Черных. — 2-е изд. — Х., 2007.
