ЕМУЛЬСІЇ (лат. emulsio < лат. emulgere — видоювати; однією з перших вивчених Е. було молоко) — вільнодисперсні системи, в яких дисперсійне середовище і дисперсна фаза рідкі. Умовою утворення Е. є взаємна нерозчинність рідин, тому ці рідини повинні дуже відрізнятися за своєю полярністю. Найбільше значення мають Е., в яких одна з фаз — вода. Другу фазу утворює неполярна чи малополярна рідина, яку незалежно від природи називають олією. Дисперсність Е. змінюється у широких межах — від краплин розміром 10–7 м до таких, які можна побачити неозброєним оком. Е. одержують головним чином шляхом механічного диспергування (струшуванням, енергійним перемішуванням, дією ультразвуку), а також витискуванням рідини через тонкі отвори під високим тиском. Застосовують і конденсаційні методи заміни розчинника та взаємної конденсації пари, що дозволяє отримати високодисперсні системи, у т.ч. й фармацевтичні.
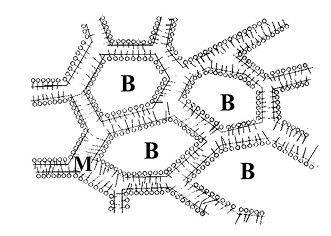
За полярністю фаз розрізняють два типи Е.: 1) прямі (Е. першого роду), які складаються з полярного дисперсійного середовища (вода) і неполярної дисперсної фази (олія) та позначаються о/в; 2) зворотні (Е. другого роду), в яких дисперсійне середовище неполярне (олія), а дисперсна фаза полярна (вода), та позначаються о/м. Тип Е. легко встановити за властивостями дисперсійного середовища. Якщо Е. типу м/в не змочує гідрофобну поверхню, розбавляється водою, забарвлюється водорозчинним барвником (напр. метиленовим синім) і виявляє значну електричну провідність, то це Е. типу о/в. За концентрацією дисперсної фази Е. розділяють на розбавлені — з концентрацією дисперсної фази не більше 0,1% об’єму Е.; концентровані — з концентрацією від 0,1 до 74% об’єму; висококонцентровані — із вмістом дисперсної фази понад 74% об’єму (максимальна концентрація, коли в Е. існують недеформовані сферичні краплини). При вищій концентрації відбувається деформування краплин, вони набувають форми багатогранників, розділених тонкими плівками дисперсійного середовища. Під мікроскопом такі Е. нагадують бджолині соти. Висококонцентровані Е. мають властивості гелів. Вони не течуть і не здатні до седиментації.
Е., як і всі колоїдні й мікрогетерогенні системи, агрегативно нестійкі внаслідок великого надлишку поверхневої енергії на міжфазній поверхні. Агрегативна нестійкість їх виявляється у довільному злипанні крапель — коалесценції, яка може призвести до повного розшарування Е. Від коалесценції відрізняється процес оборотної коагуляції — флокуляції, коли утворюються агрегати краплин, які не злипаються, а зберігають свою індивідуальність і за певних умов знову розходяться. Седиментація Е. — спливання або осідання краплин дисперсної фази залежить від їх дисперсності, різниці в густині фаз, в’язкості середовища. Високодисперсні Е. седиментаційно більш стійкі, ніж грубодисперсні.
Агрегативна стійкість Е. тісно пов’язана з концентрацією дисперсної фази. У розбавлених Е. властивості майже не відрізняються від властивостей ліофобних золів: частинки дисперсної фази несуть заряд, вплив електролітів відповідає правилу Шульце — Гарді, існує критичний ζ-потенціал, багатозарядні іони змінюють знак заряду частинок. Розбавлені Е. зазвичай утворюються без введення в систему емульгаторів. Заряд на частинках таких Е. виникає внаслідок адсорбції іонів неорганічних електролітів, які можуть бути присутні в середовищі у дуже малій кількості, або внаслідок адсорбції водневих і гідроксильних іонів води. У розбавлених Е. зіткнення частинок відбуваються рідко, що теж підвищує їх агрегативну стійкість. Для утворення концентрованої Е. в системі необхідний емульгатор (речовина, що надає стійкості Е.), який знижує поверхневий натяг на межі поділу фаз. За правилом Банкрофта, емульгатори, які краще розчиняються у воді, ніж у маслі, стабілізують прямі Е., і, навпаки, якщо розчинність емульгатора у маслі більша, ніж у воді, він стабілізує Е. типу в/о. Е. типу о/в стабілізують Е. з числом гідрофільно-ліпофільного балансу 8–18 (див. Поверхнево-активні речовини), зворотні емульсії — з числами 3–6. Перші емульгатори називають гідрофільними, другі — гідрофобними. Сильну емульгувальну здатність мають мила з числом атомів вуглецю (nc) від 12 до 18 (олеати, стеарати). Вони адсорбуються на міжфазній межі й утворюють структурні шари, звернені іоногенними групами до води, а неполярними ланцюгами — до масла. Таким чином, стабілізувальна дія емульгатора полягає не тільки і не стільки в зниженні поверхневого натягу, скільки в утворенні структурно-механічного бар’єра. Структурно-механічний бар’єр утворюють також тверді емульгатори — порошки. Напр., якщо струшувати мінеральне масло з водою в присутності глини, то спочатку утворюються два типи емульсій: о/в і в/о. Крім низькомолекулярних ПАР і порошків, ефективними емульгаторами є високомолекулярні ПАР (желатин, сапоніни, полівінілові спирти та ін.). Ці речовини утворюють на межі розділення фаз тривимірні сітки. Високомолекулярні емульгатори також підпорядковуються правилу Банкрофта, оскільки сітка утворюється завжди з того боку межі розділення, де високомолекулярна ПАР розчинна. Ця рідина і стає неперервною фазою.
Для одержання лікарських Е. особливо широко застосовують оксіетильовані неіоногенні ПАР — твіни і плюроніки. Речовини типу плюронік використовують для одержання дисперсій ЛП, які вводять у систему кровообігу. Вони були застосовані для емульгування перфторвуглеводнів, запропонованих для перенесення кисню у «штучній крові». ПАР типу твін використовують найчастіше у лікарських Е. для зовнішнього застосування. Важливо знати, який тип Е. утвориться при сумісному диспергуванні масла і води. Якщо об’єми фаз приблизно однакові, то спершу утворюються і крапельки масла, і крапельки води. Тому менш стійкі краплі коалесціюють, утворюючи дисперсійне середовище, а більш стійкі виживають і стають дисперсною фазою. Тип Е. залежить від гідрофільно-ліпофільного балансу емульгатора, гідрофільний емульгатор дає пряму Е., а гідрофобний — зворотну. Вплив гідрофільно-ліпофільного балансу на тип Е. особливо чітко проявляється у явищі обернення фаз Е. (тобто перехід Е. прямого типу в Е. зворотного типу і навпаки). Нерідко виникає необхідність руйнування Е. Напр. до руйнування призводять суто механічні дії: розмішування і збовтування. Прикладом є одержання вершкового масла при збиванні вершків, центрифугування при відділенні вершків від молока. Розбавлені Е. можна деемульгувати додаванням електроліту. Руйнування Е. можна здійснити за допомогою деемульгаторів — ПАР, які мають більшу порівняно з емульгаторами поверхневу активність, але меншу здатність до утворення структурованих шарів. Е. мають велике значення в житті людини. Засвоєння жирів в організмі відбувається через емульгування під впливом жовчі. Молоко, яєчний білок, вершки, сметана, що знаходяться в емульгованому стані, добре засвоюються. Е. належать до рідких лікарських форм як для зовнішнього, так і для внутрішнього застосування. При пероральному застосуванні доцільно використовувати прямі Е., а при зовнішньому — Е. зворотного типу, тому що вода і розчинені в ній речовини не можуть проникати через шкіру. Зворотні Е., зокрема, застосовують у вигляді лікарських та косметичних мазей і кремів. Прямі Е. перфторвуглецевих сполук у воді є перспективними кровозамінниками.
Клейтон В. Эмульсии. — М., 1950; Перцов А.В., Чистяков Б.Е. Эмульсии. В кн.: Химическая энциклопедия: В 5 т. — М., 1998; Фізична і колоїдна хімія / В.І. Кабачний, Л.К. Осіпенко, Л.Д. Грицан та ін. — Х., 1999.
