ПОХІДНІ ФЕНОТІАЗИНУ — група активних речовин, в основі структури яких лежить похідне дибензотіазину або фенотіазину:
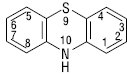
Фенотіазин застосовували в медицині як антигельмінтну активну речовину і антисептик при запальних захворюваннях сечових шляхів. Тепер його застосовують як антигельмінтну активну речовину у ветеринарії, а технічний продукт — для знищення личинок комарів. Велике значення у фармакотерапії мають П.ф., отримані шляхом модифікації молекули фенотіазину, а саме — приєднання різних радикалів у 2 та 10 положеннях.
Починаючи з 1945 р., після виявлення фармакологічної активності N-заміщених П.ф., було синтезовано велику кількість активних речовин, які мають нейролептичну, антигістамінну, холіноблокуючу, седативну, антиаритмічну та коронаророзширювальну дію. Вони схожі за хімічною структурою речовинами, що відрізняються лише замісниками фенотіазинового кільця (таблиця).
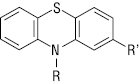
| Активна речовина |
R | R´ |
| Хлорпромазину гідрохлорид | –CH2–CH2–CH2–N(CH3)2· HCl | Cl |
| Прометазину гідрохлорид | 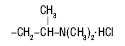 |
– |
| Трифторперазину гідрохлорид | 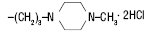 |
CF3 |
| Промазин | -CH2-CH2-CH2-N(CH3)2×HCl | – |
| Перфеназин | 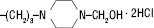 |
Cl |
| Морацизин | 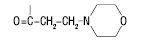 |
–NHCOOC2H5 |
Існує декілька класифікацій П.ф: коли їх поділяють на речовини, які містять або не містять атомів флюору в молекулах. Активні речовини, які не містять атомів флюору в молекулах, у свою чергу, поділяють на три групи: 1) фенотіазини з діалкіламіноалкільними замісниками в положенні 10 (хлорпромазин, промазин, левомепромазин, алімемазин, прометазин, динезин та ін.); 2) фенотіазини з піперазиновими циклами в бічних ланцюгах у положенні 10 (прохлорперазин, тіопроперазин, перфеназин, метофеназат, тіетилперазин та ін.); 3) фенотіазини з піперидиновими циклами в бічних ланцюгах у положенні 10 (периціазин, тіоридазин та ін.). До П.ф. з атомами флюору в молекулі належать трифторперазину гідрохлорид, флуфеназину гідрохлорид, флуфеназин деканоат. Окрему групу становлять фенотіазини з ацильними замісниками в положенні 10 (фторацизин, морацизин, нонахлазин та ін.). За фізичними властивостями П.ф. — це білі або з ледь жовтуватим чи рожевим відтінком кристалічні речовини без запаху; дуже легко- або легкорозчинні у воді, легкорозчинні або розчинні у спирті, практично нерозчинні в етері. Значення рН водних розчинів — у межах 3–4 (алкілпохідні) і 4–6 (ацилпохідні); трифторперазину гідрохлорид — гігроскопічний. Для ідентифікації АФІ П.ф. використовують фізичні методи визначення (Tпл речовин, їх основ і пікратів основ), фізико-хімічні методи (ІЧ-, УФ- та ЯМР-спектроскопія, ТШХ, ВЕРХ та ін.) та хімічні реакції, які ґрунтуються на кислотно-основних і відновних властивостях. Завдяки наявності атома сульфуру похідні фенотіазину легко окиснюються. Для їх окиснення використовують кислоту сірчану концентровану, бромну воду, кислоту азотну, заліза (ІІІ) хлорид та ін., при цьому утворюються забарвлені продукти. Зазначені реакції малоспецифічні. Залежно від умов утворюються суміші продуктів окиснення: напр. 9-S-оксид (а) і 9,9-S-діоксид (б):
Згідно з вимогами ДФУ окиснення проводять кислотою азотною концентрованою, при цьому прометазину гідрохлорид утворює оранжеве забарвлення та оранжево-червоний осад; трифторперазину гідрохлорид — темно-червоне забарвлення, яке переходить у блідо-жовте. З кислотою сірчаною концентрованою утворюють: хлорпромазину гідрохлорид — малинове забарвлення; прометазину гідрохлорид — червоне або червоно-оранжеве забарвлення; промазин — червоно-оранжеве забарвлення.
Найбільш специфічним реактивом є бромна вода, з якою субстанції утворюють: трифторперазину гідрохлорид — червоне забарвлення; хлорпромазину гідрохлорид — прозорий світло-малиновий розчин; прометазину гідрохлорид — каламутний темно-вишневий розчин із зависсю; промазин — прозорий коричнево-червоний розчин; морацизин — спочатку світло-бузковий, а потім яскраво-фіолетовий розчин. Вважається, що забарвлені продукти зумовлені утворенням пербромпохідних фенотіазину:
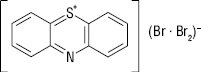
Більшість активних речовин П.ф. — солі сильних мінеральних кислот і органічних нітрогеновмісних основ. Основи виділяються із розчинів дією розведених розчинів гідроксидів та карбонатів лужних металів, амоніаку у формі аморфних або олієподібних сполук. Як солі азотистих основ вони взаємодіють із загальноалколоїдними осадовими реактивами (Майєра, Драгендорфа, Бушарда, Вагнера, таніном, пікриновою кислотою та ін.). Деякі осади добре кристалізуються та мають певну Tпл. Деякі комплексні сполуки препаратів цієї групи з реактивом Драгендорфа мають характерну форму кристалів, що використовується у токсикологічному аналізі. З паладію (ІІ) хлоридом сполуки цього ряду утворюють комплекси синього кольору, що використовують для кількісного фотоколориметричного визначення лікарських форм. У хлористоводневих солях визначають хлорид-іон. При цьому на розчин АФІ діють розчином лугу для осадження основи, а у фільтраті після додавання кислоти нітратної визначають хлориди реакцією з розчином срібла нітрату. За безпосередньої дії на речовину срібла нітратом окиснюється система фенотіазину і можуть утворюватися нітрати, нерозчинні у воді. Сульфур фенотіазинового циклу визначають після мінералізації (суміш натрію карбонату і натрію нітрату) дією розчину барію хлориду.
Для кількісного визначення солей активних речовин П.ф. рекомендується метод кислотно-основного титрування в суміші спирту та 0,01 М розчину кислоти хлористоводневої з потенціометричним фіксуванням кінцевої точки титрування. Відомі методики кількісного визначення цієї групи сполук методами кислотно-основного титрування у неводному середовищі, визначення азоту після мінералізації кислотою сульфатною, цериметрії, йодометрії, йодохлорометрії, спектрофотометрії, фотоколориметрії, екстракційної спектрофотометрії (за реакцією взаємодії АФІ з кислотними індикаторами, такими як метиловий оранжевий, бромтимоловий синій, бромфеноловий синій) та ін.
Розчини з П.ф. для ін’єкцій стабілізують додаванням антиоксидантів (суміш натрію сульфіту, натрію бісульфіту, кислоти аскорбінової). П.ф. здатні проникати в організм крізь дихальні шляхи, шкіру і слизову оболонку. При цьому вони викликають алергічні реакції (свербіж і набряк слизової оболонки, шкіри рук, зниження АТ, стан депресії тощо). Тому необхідно суворо дотримуватися техніки безпеки в роботі, запобігаючи потраплянню АФІ на шкіру та слизову оболонку. Роботу слід здійснювати в гумових рукавичках, під витяжкою. Після закінчення роботи руки миють холодною підкисленою водою, без мила, щоб запобігти виділенню на шкірі основ П.ф. Між структурою замісників та фармакологічною дією виявляється чітка залежність: якщо в 10-му положенні перебуває ліпофільне угрупування, що містить третинний нітроген в аліфатичному залишку, то речовина має нейролептичну, седативну та протиалергічну дію. Якщо ж це угрупування гідрофільне (карбоксильна група), то виявляється коронаророзширювальний і антиаритмічний ефект. На цей час до П.ф. належать седативні й нейролептичні (хлорпромазин, левомепромазин, прохлорперазин, флуфеназин та ін.), холінолітичні (динезин та ін.), антигістамінні (промазин, піпольфен), протиблювотні (алімемазин, тіетилперазин, тіопроперазин та ін.), антидепресивні (фторацизин та ін.), серцево-судинні (морацизин, нонахлазин та ін.) АФІ.

Препарати цієї групи під час застосування всмоктуються в повному обсязі. Cmax досягається через 2–4 год, при в/м уведенні — через 1–2 год. У плазмі крові П.ф. зв’язуються із білками на 99%; проникають через гематоенцефалічний бар’єр. Метаболізуються в печінці. T½ становить 15–30 год. Екскретуються нирками переважно у вигляді метаболітів. Токсична концентрація у крові — 1–2 мг/л, летальна доза — 3–12 мг/л. АФІ фенотіазинового ряду, як і інші психотропні, антигістамінні та серцево-судинні речовини, крім власного терапевтичного ефекту, виявляють побічний і токсичний вплив. Мають кумулятивні властивості й довго виводяться з організму. Напр., терапевтична доза хлорпромазину гідрохлориду (50 мг) виводиться з організму протягом 14–20 днів. Летальні випадки можливі при застосуванні у звичайних терапевтичних дозах. Отруєння П.ф. значною мірою залежить від віку, статі, дози прийнятих ЛЗ. Біотрансформація П.ф. відбувається за основним типом метаболізму: сульфоокиснення, деметилювання, утворення N-оксиду, гідроксилювання тощо. Головним метаболітом, загальним для всіх П.ф., є сульфоксид.
Чутливість речовин П.ф. до окиснення зумовлює необхідність їх зберігання в герметичних склянках темного скла, у захищеному від світла місці.
Літ.: Беликов В.Г. Фармацевтическая химия. — Пятигорск, 1996; ДФ України. — Х., 2001; Машковский М.Д. Лекарственные средства. — М., 2012; Туркевич М.М., Владзімірська О.В., Лесик Р.Б. Фармацевтична хімія. — Вінниця, 2003; Химическая энциклопедия: В 5 т. / Ред. И.Л. Кнунянц и др. — М., 1988.
