ПУЛЬМОПРОТÉКТОРИ (лат. рulmo — легеня або те, що легше води, + лат. protegere — покривати, захищати) — ЛП, які підвищують стійкість легенів до впливу патологічних факторів, компенсують дефіцит ендогенного сурфактанта, сприяють відновленню ушкодженої легеневої тканини при захворюваннях дихальної системи та профілактиці ателектазу, пневмо- та фібросклерозу тощо. До П. належать сурфактанти, стимулятори синтезу сурфактанта (амброксол, топічні кортикостероїди), ферментні препарати (ацетилцистеїн, карбоцистеїн), антагоністи аденозину (амінофілін, метиламід етилімідазолдикарбонат) та ін.
Найчастіше як П. використовують препарати, отримані з екзогенного легеневого сурфактанта, що складається переважно з фосфоліпідів і білків, виконує широкий спектр захисних функцій, головною серед яких є антиателектатична (захист від спадання альвеол). Недостатня зрілість сурфактанта у новонароджених призводить до спадання альвеол і розвитку синдрому гострої дихальної недостатності — респіраторний дистрес-синдром новонароджених (РДСН). Сурфактант знижує поверхневий натяг в альвеолах, забезпечує їх стабільність у процесі дихання, запобігає спаданню в кінці фази видиху, забезпечує адекватний газообмін, виконує протинабрякову функцію. Крім того, сурфактант бере участь в антибактеріальному захисті альвеол, підвищує активність альвеолярних макрофагів, покращує функцію мукоциліарної системи, інгібує низку медіаторів запалення при синдромі гострого ушкодження легень (СГУЛ) і гострому респіраторному дистрес-синдромі у дорослих (ГРДС). При недостатній продукції власного (ендогенного) сурфактанта використовують препарати екзогенного сурфактанта, отримані з легенів тварин (великої рогатої худоби, свині) або синтетичним шляхом. Хімічний склад легеневого сурфактанта ссавців має багато спільного з сурфактантом людини, який містить фосфоліпіди — 80–85%, білки — 10% і нейтральні ліпіди — 5–10% (табл. 1).
Таблиця 1. Фосфоліпідний склад альвеолярного сурфактанта людини
| Фосфоліпіди сурфактанта | Вміст,% |
| Фосфатидилхолін | 76–80,5 |
| У т.ч. дипальмітоїлфосфатидилхолін | 44,7–66 |
| Фосфатидилгліцерол | 9–12 |
| Фосфатидилінозитол | 2,6–3,9 |
| Фосфатидилетаноламін | 2,3–3,3 |
| Сфінгомієлін | 1,5–2,7 |
| Фосфатидилсерин | 0,9–1 |
| Інші | 1,5–3,4 |
Фосфоліпіди та білок сурфактанта беруть участь у процесі рециклювання й метаболізму (в альвеолоцитах II типу). Сурфактант містить 4 класи білків (Sр-A, Sp-В, Sp-С, Sp-D), кожен з яких кодується власним геном. Основну масу білків становить Sp-А. Препарати ендогенного сурфактанта різного походження дещо відрізняються за вмістом фосфоліпідів і білків. Сурфактант синтезується й секретується альвеолоцитами II типу (а-II). На альвеолярній поверхні сурфактант складається з тонкої фосфоліпідної плівки та гіпофази, в якій містяться мембранні включення. Це дуже динамічна система — щогодини секретується понад 10% усього пулу сурфактанта.
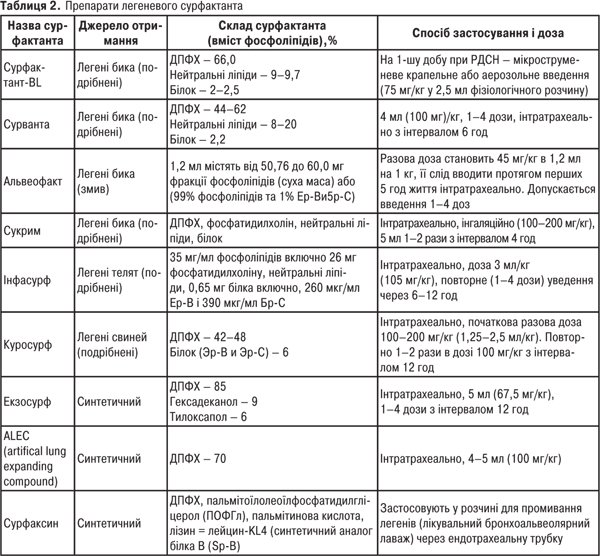
Раннє використання препаратів сурфактанта при РДСН дозволяє значно знизити смертність (на 40–60%), а також частоту полісистемних ускладнень (пневмоторакс, інтерстиціальна емфізема, кровотечі, бронхолегенева дисплазія та ін.), пов’язаних з неонатальним періодом у недоношених дітей. Останнім часом препарати легеневого сурфактанта почали застосовувати в лікуванні СГУЛ/ГРДС та інших патологій легень. Відомі наразі препарати легеневого сурфактанта відрізняються за джерелом отримання та вмістом у них фосфоліпідів (табл. 2).
Багатоцентрові клінічні випробування підтвердили ефективність використання препаратів легеневого сурфактанта в лікуванні критичних станів та інших захворювань органів дихання.
Механізм дії препаратів легеневого сурфактанта. Дипальмітоїлфосфатидилхолін (ДПФХ) — основний компонент сурфактанта, який знижує поверхневий натяг в альвеолах. Фосфатидилгліцерол (ФГл) відіграє важливу роль у поширенні сурфактанта по альвеолярній поверхні легенів і взаємодії кальцію з білками сурфактанта. Сурфактантний білок Sp-A міцно зв’язується з ДПФХ, бере участь у формуванні «тубулярного мієліну» — мембранного компонента гіпофази сурфактанта, а також в імунологічному захисті альвеол, вступаючи у взаємодію з різними бактеріями та вірусами. Sp-B також необхідний для формування решітчастих мембранних утворень сурфактанта і бере активну участь у доставці фосфоліпідів на поверхню альвеол на межу розподілу фаз «повітря-рідина». Sp-С є компонентом тільки легеневого сурфактанта, стабілізує поверхневу плівку сурфактанта, є маркером. Sp-D зв’язує фосфоліпіди сурфактанта, виконує важливу захисну роль, активізує функцію альвеолярних макрофагів.
Фармакокінетика екзогенних сурфактантів недостатньо вивчена. Кожен препарат легеневого сурфактанта є багатокомпонентною сполукою, що значною мірою ускладнює дослідження фармакокінетики як кожної її складової, так і препарату в цілому. При прямій інтратрахеальній інстиляції 70–90% уведеного сурфактанта досягають дистальних дихальних шляхів й альвеол. Препарат рівномірно та швидко розподіляється по поверхні альвеол. При цьому важливе значення мають методика введення, доза та властивості препарату, що вводиться, положення хворого, наявність або відсутність бронхіальної обструкції, стадії хвороби. Невелика кількість сурфактанта залишається у верхніх дихальних шляхах й ендотрахеальній трубці. Уведений екзогенний сурфактант виявляють не лише в альвеолах, але й у рідинному шарі сурфактанта (гіпофазі), що їх вистеляє, а також в альвеолоцитах II типу. Отже, компоненти екзогенного сурфактанта мають ту саму фармакокінетику, що й складові природного сурфактанта. При інтратрахеальному введенні сурфактанта основну частину препарату виявляють в легенях. Через 48 год після введення реєструють лише сліди ліпідів сурфактанта в сироватці крові та в інших органах. Т½ препаратів сурфактанта становить 65–67 год.
Основне клінічне значення препаратів легеневого сурфактанта визначається їх ефективністю при тяжких респіраторних захворюваннях, пов’язаних з первинним або вторинним дефіцитом сурфактанта. До них насамперед належать такі захворювання та синдроми: РДСН, що виникає внаслідок незрілості легенів і, зрештою, вираженого дефіциту сурфактанта. Недостатній синтез сурфактанта альвеолоцитами II типу і його швидка інактивація призводять до підвищення поверхневого натягу в альвеолах, їх спадання (ателектаз), гіповентиляції й недостатньої оксигенації крові, розвитку гіперкапнії та гіпоксії. Порушення в системі легеневого кровообігу викликають ушкодження всіх компонентів аерогематичного бар’єру (епітелій, інтерстицій, ендотелій), набряк легенів і приєднання інфекції, що спричиняє ці зміни РДСН. Синдром аспірації меконію у новонароджених виникає внаслідок потрапляння меконію (калових мас плода) у дихальні шляхи, що призводить до порушення синтезу сурфактанта, його інактивації компонентами меконію, спадання альвеол і розвитку запалення. Призначення сурфактанта сприяє зниженню тяжкості захворювання, запобігає розвитку гострої дихальної недостатності. СГУЛ і ГРДС дорослих — компоненти поліорганної недостатності, які розвиваються внаслідок вторинного ушкодження легенів, у тому числі всі компоненти аерогематичного бар’єру і альвеолярного сурфактанта. Важливе місце в патогенезі СГУЛ/ГРДС належить запальній реакції та вторинному дефіциту сурфактанта, що виникає внаслідок місцевого (пневмонія, вдихання токсичних речовин) або системного (множинна травма, сепсис, тривала штучна вентиляція легень, ускладнення після штучного кровообігу та при післятрансфузійному синдромі) ушкодження легенів із розвитком запальної реакції. Дефіцит сурфактанта призводить до спадання альвеол, дрібних дихальних шляхів, набряку легенів, розвитку гострої дихальної недостатності.
Пневмонія супроводжується ушкодженням альвеолярної паренхіми, набряком легенів з виходом білків плазми крові в альвеоли, що пригнічує дію сурфактанта і призводить до спадання альвеол. Дослідження сурфактанта при пневмонії показали значне зниження вмісту різних фосфоліпідних фракцій і білка у складі бронхоальвеолярного лаважу (ФГ, ФГл, ДПФХ, Sp-A). Призначення сурфактанта покращує газообмін, сприяючи розправленню альвеол, що спали.
Туберкульоз легенів, особливо його поширені форми, викликає глибокі порушення в сурфактантній системі легенів, численні деструктивні й ателектатичні зміни альвеолярної паренхіми, особливо в ділянках легенів, що межують з великими туберкульозними фокусами (інфільтрати, каверни та ін.). Застосування препаратів сурфактанта в комплексному лікуванні туберкульозу дозволяє знизити частоту виникнення сурфактантозалежних змін у легенях, підвищити поверхневоактивні властивості легеневого сурфактанта і сприяє швидшому зворотному розвитку запальних змін.
Розроблено такі принципи сурфактантної терапії: вичерпна базова терапія; використання принципів неушкоджувальної механічної вентиляції; ранній початок сурфактантотерапії (перші години, дні з моменту розвитку РДСН), при індексі оксигенації РаO2/РO2 <200 мм рт. ст.; ендобронхіальне болюсне введення препарату в ефективній дозі та друге введення через 6–8 год у разі позитивної відповіді на перше введення; сурфактантотерапію при позитивній відповіді на перше введення необхідно проводити до досягнення індексу оксигенації >300 мм рт. ст., стійкого клініко-рентгенологічного поліпшення.
Протипоказання й застереження. Препарати легеневого сурфактанта зазвичай добре переносяться. Для запобігання ускладненням уведення сурфактанта слід проводити в спеціалізованому відділенні лікарями, які мають відповідну підготовку та досвід застосування препаратів сурфактанта. В окремих випадках можлива закупорка ендотрахеальної трубки слизом. Швидке введення емульсії препарату може призвести до обтурації неповністю розкритих дихальних шляхів, бронхіальної обструкції чи викликати рефлюкс сурфактанта. У рідкісних випадках можлива легенева кровотеча, головним чином у новонароджених з вираженими ознаками незрілості легенів. Відразу після введення препарату сурфактанта можливе швидке збільшення розтяжності легенів, що вимагає корекції показників вентиляції. Поліпшення газообміну може спричинити зростання концентрації кисню в крові. За цих умов необхідно знизити концентрацію кисню в газовій суміші, щоб попередити гіпероксемію. Досвід застосування препаратів сурфактанта свідчить, що для отримання максимального ефекту від сурфактантотерапії та зниження частоти ускладнень, пов’язаних зі штучною вентиляцією легенів і ускладненим неонатальним періодом, у недоношених новонароджених із РДСН обов’язковою є попередня стабілізація центральної гемодинаміки і показників тканинної трансфузії (лікування гіповолемії, анемії, олігурії). Протипоказання фактично не встановлені, однак слід мати на увазі можливу підвищену чутливість до будь-яких компонентів препарату легеневого сурфактанта. Взаємодія з іншими ЛП. Будь-яких реакцій взаємодії препаратів легеневого сурфактанта з іншими ЛП не встановлено.
Ерохина В.В., Романова Л.К. Сурфактантная система легких. Клеточная биология легких в норме и при патологии. — М., 2000; Рациональная фармакотерапия заболеваний органов дыхания: Рук. для практикующих врачей. Т. 5 / А.Г. Чучалин, С.Н. Авдеев, В.В. Архипов, С.Л. Бабак. — М., 2004; Розенберг О.А., Осовских В.В., Гранов Д.А. Сурфактант-терапия дыхательной недостаточности критических состояний и других заболеваний легких. — СПб., 2002; Artificial surfactant therapy in hyaline-membrane disease / Т. Fujiwara, H. Maeta, S. Chida et al. // Lancet. — 1980; Biochemical composition of adult human lung surfactant / S.A. Shelley, J.U. Balis, J.E Pacida et al. // Lung. — 1982; Bunt J.E.N. Surfactant therapy stimulates endogenous surfactant synthesis in premature infants // Crit. Care Med. — 2000; Lachmann B. Surfactant therapy // Resuscitation. — 1989; Lewis J.F., Jobe A.H. Surfactant and the adult respiratory distress syndrome // Amer. Rev. Respir. Dis. — 1993; Person A., Rust K., Chang D. A pneumocytederived collagenous surfactant — associated protein. Evidence for heterogeneity of collagenous surfactant proteins // Biochemistry. — 1998. — № 23.