ГІДРОГЕН ФЛУОРИД (Hydrogenii fluoridum; син.: фторид (флуорид) водню, фтористий водень, гідроген фторид). Ткип = 19,43 °С, Тпл = –83,37 °С. Нижче за 19,43 °С — безбарвна легко рухома рідина, вище за цю температуру — безбарвний газ із різким запахом. Густина рідкого Г.ф. — 0,98 г/см3 (при 12 °С). Такі високі значення Tкип та Тпл Г.ф. порівняно з показниками в ряду HІ-HCl зумовлені високою полярністю молекул Г.ф., яка призводить до їх значної асоціації. У газоподібному Г.ф. згідно з даними щодо дифракції електронів виявлено зигзагоподібні (<40 ± 5°) ланцюжки молекул Г.ф. змінної довжини з відстанню між атомами сусідніх ланок ланцюга 1,55 ± 0,06 Å (для порівняння: відстань між атомами у молекулі 1,06 ± 0,06 Å). У твердому стані Г.ф. кристалізується у ромбічні кристали. Він змішується з водою в усіх співвідношеннях з виділенням значної кількості теплоти. Водні розчини Г.ф. мають назву плавикової кислоти. Густина цих розчинів із підвищенням концентрації Г.ф. змінюється нелінійно, її максимум відзначається при 77%. У вільному стані Г.ф. у природі не виявляють.
У промисловості Г.ф. одержують дією концентрованої H2SO4 на плавиковий шпат CaF2:
CaF2 + H2SO4(к.) = 2HF↑ + CaSO4.
З використанням такого методу одержують 98–99% Г.ф. та кубовий залишок у вигляді 40–42% розчину плавикової кислоти. Його одержують також із SiF4 — відходів виробництва мінеральних добрив за схемою:
NH4F NH3+H2O H2SO4
SiF4 (NH4)2SiF6 NH4F (NH4HF2) HF
У лабораторних умовах Г.ф. одержують нагріванням безводного КHF2 у срібній апаратурі при 500 °С. Для повного зневоднення рідкого Г.ф. через нього пропускають F2 або застосовують електроліз. З воднем фтор взаємодіє з вибухом з утворенням Г.ф.:
H2 + F2 = 2HF.
Хімічні властивості Г.ф. визначаються в основному за такими факторами: сильною кислотністю безводного Г.ф. (для 100% Г.ф. функція кислотності Гаммета Но = –10,2) та здатністю до утворення комплексних сполук. Завдяки специфічній здатності до комплексоутворення Г.ф. реагує не лише з основами, а й з багатьма кислотними оксидами, оксигенвмісними кислотами та їх солями. Іонний добуток безводного Г.ф. дуже малий ([H2F+][F–] < 2 · 10–10), але при розчиненні у ньому будь-якої речовини дисоціація різко збільшується за рахунок сольватації іона гідрогену молекулами розчиненої речовини, тобто електролітично дисоціює розчинник, а не розчинена речовина (це кардинальна відмінність безводного Г.ф. від води):
H2O + HF = H3O+ + F–
CH3COOH + HF = CH3COOH+2 + F–
C2H5OC2H5 + HF = (C2H5)2OH+ + F–.
Специфічною особливістю Г.ф. є здатність інтенсивно реагувати з багатьма силікатними матеріалами:
у газовій фазі
SiO2 + 4HF(г.) = SiF4↑ + 2H2O;
у водних розчинах
SiO2 + 6HF(р) = H2[SiF6] + 2H2O.
На відміну від інших гідрогенгалогенідів, водні розчини Г.ф. є слабкими електролітами, при цьому його константа дисоціації залежить від концентрації. Це пояснюється наявністю міжмолекулярних водневих зв’язків, за рахунок яких Г.ф. знаходиться в асоційованому стані (HF)n, коли n змінюється від 1 до 4 (для водних розчинів здебільшого n = 2). Це можна відобразити таким чином:
HF 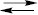 H+ + F– Kд1=7,2 ·10-4,
H+ + F– Kд1=7,2 ·10-4,
HF + F–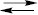 HF–2 Kд2=3,94.
HF–2 Kд2=3,94.
Отже, плавикова кислота є єдиною з гідрогенгалогенідних кислот, яка утворює кислі солі (напр. КHF2). Солі плавикової кислоти мають назву фторидів (флуоридів). Але в багатьох випадках здатність Г.ф. реагувати з іншою речовиною обмежується утворенням щільної плівки нерозчинного фториду. Так Mg, Al, Zn, Cd, Fe, Ni та деякі інші метали не витісняють водень з безводного Г.ф. завдяки утворенню такої плівки, не розчинної у Г.ф., на поверхні металу. NiF2, крім того, нерозчинний і у водних розчинах Г.ф., що застосовується при створенні хімічної апаратури, яка практично не кородує у флуоровмісних середовищах. Добрерозчинними у воді є фториди лужних металів та аргентуму, а також амонію. Г.ф. бурхливо реагує з ангідридами та галогенагідридами неорганічних кислот з утворенням фторокислот або їх фторангідридів:
SO3+ HF = HSO3F
PCl5 + 6HF = HPF6+ 5HCl
SbCl3 + 3HF = SbF3 + 3HCl
UO2 + 4HF = UF4 + 2H2O.
Г.ф. реагує з багатьма органічними сполуками. При дії Г.ф. на полігалогеналкани атоми іншого галогену в них заміщуються атомами F. HF легко приєднується до кратного зв’язку органічних сполук, у деяких випадках ініціюючи їх полімеризацію. При цьому взаємодія відбувається згідно з правилом В.В. Марковникова (якщо реакція проходить за іонним механізмом):
| δ+ δ- δ+ δ- | CH3-CHF-CH2 90% | |
| CH3-CH=CH2 + HF | CH3-CH2-CH2F 10% |
Зі спиртами Г.ф. у присутності водовіднімаючих реагентів утворює відповідні галогенпохідні. З простими ефірами Г.ф. утворює онієві солі, напр.:
С2Н5
С2Н5
Ö:Н F–
+
Г.ф. гідролізує аміди до відповідних кислот, з амінами утворює четвертинні солі. Ароматичні фторпохідні одержують взаємодією Г.ф. у суміші з HNO2 та ароматичним аміном (проміжним продуктом при цьому є діазосполуки).
Випари Г.ф. сильно подразнюють слизові оболонки та дихальні шляхи. Хронічні отруєння зумовлені токсичністю фторид-іона, який є протоплазменною отрутою (блокує роботу ферментів — холінестерази, аденозинтрифосфатази та ін.). Потрапляння на шкіру як безводного, так і водного Г.ф. викликає дерматит. У фармацевтичній практиці застосовують похідні Г.ф. Так, NaF є складовою деяких зубних паст (зміцнює емаль), а також входить до складу полівітамінних препаратів (напр. Оліговіту). NaF знижує резорбцію кісткової тканини. Органічні похідні Г.ф. застосовують при створенні кровозамінних препаратів.
Краткая химическая энциклопедия. — М., 1988; Левитин Е.Я., Бризицкая А.Н., Клюева Р.И. Общая и неорганическая химия. — Х., 2002; Рысс И.Г. Химия фтора и его неорганических соединений. — М., 1956; Фтор и его соединения. — М., 1953. — Т. 1.
