Гліцерин (ДФУ), гліцерол, Glycerolum (Ph Eur), Glycerol (BP), Glycerin (USP), Propane-1,2,3-triol, (CAS № 56-81-5). С3Н8O3. Г — це сиропоподібна рідина, липка на дотик, солодка на смак, без запаху, прозора, безбарвна або майже безбарвна, дуже гігроскопічна, поглинає вологу з повітря (до 40% за масою).
CH2(OH)CH(OH)CH2OH Мол. м. 92,09
![]()
Має такі властивості: Тпл = 17,9 °С, Ткип = 290 °С (з незначним розкладанням); 1,260, 1,4740. Змішується з водою, етанолом, метанолом у будь-яких співвідношеннях, мало розчинний в ацетоні, етилацетоні (1 : 11), практично нерозчинний в етері (1 : 500), хлороформі й жирних оліях. При змішуванні Г. з водою виділяється тепло і відбувається контракція (зменшення об’єму), яка досягає найбільшого значення для суміші, що містить 57% Г.; гліцерино-водні розчини замерзають при низьких температурах, напр. суміш, яка містить 66,7% Г., замерзає при –46,5 °С. Моно- і дипохідні Г. існують у вигляді двох структурних ізомерів, а похідні Г. типу CH2ХCH(OH)CH2OH або CH2ХCHХCH2OH — у вигляді оптичних ізомерів. Кислотні властивості Г. виражені сильніше, ніж в одноатомних спиртах. Г. утворює три ряди похідних при взаємодії з активними металами (Na, Al, Mg), лугами, гідроксидами важких металів. При взаємодії Г. з галогеноводневими кислотами або галогенідами фосфору утворюються моно- або дигалогенгідрини; з неорганічними та органічними кислотами — повні або неповні естери; при дегідратації — акролеїн. Як і інші спирти, Г. окиснюється. Залежно від природи окисника та умов окиснення можна отримати гліцериновий альдегід — CH2(OH)CH(OH)CНО, гліцеринову кислоту — CH2(OH)CH(OH)CООН, тартронову кислоту — (НООС)2СНОН, дигідроксіацетон — НОСН2СОСН2ОН, мезоксалеву кислоту — (НООС)2СО. Під дією KMnO4 або K2Cr2O7 Г. окиснюється до СО2 і Н2О.
Гліцерин міститься в природних жирах та оліях у вигляді змішаних тригліцеридів карбонових кислот. У промисловості Гліцерин отримують омиленням харчових жирів, які розщеплюються на Г. та жирні кислоти за наявності каталізаторів (кислот, лугів, ферментів).
Гліцерин також отримують синтетичним (хлоргідринним) методом:
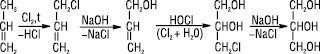
Зберігають Гліцерин у герметичній тарі з нержавіючої сталі.
Широко використовують у фармацевтичній практиці (з питомою вагою 1,225–1,235, що відповідає вмісту 86–90% чистого Г. і 14–10% води) як зволожувальний і пом’якшувальний агент, для підвищення адгезії, коригування реологічних параметрів в’язких систем та їх вологоутримуючих властивостей. Сприяє покращанню проникності шкіри. При високій концентрації виявляє бактеріостатичні властивості.
У суміші з водою і спиртом є розчинником для деяких діючих речовин (іхтіолу, таніну), входить до складу желатино-гліцеринових і мильно-гліцеринових супозиторних основ; спирто-гліцерино-водну суміш (1 : 3 : 6) використовують для попереднього розтирання сухих і густих екстрактів при виготовленні ЛП.
Гліцерин виявляє пенетруючу та власне фармакологічну дію (проносну, дерматопротекторну, зволожувальну, пом’якшувальну, дегідратуючу (осмотичну), обволікаючу, в’яжучу) і використовується як АФІ (фармакологічна група D02A Х, А06A G04 — проносні препарати). Застосовується при запорах, тріщинах анального отвору, набряках головного мозку, при порушеннях мозкового кровообігу (внутрішньо), для пом’якшення шкіри та обробки слизових оболонок (у чистому вигляді при нанесенні на шкіру чинить подразливу дію, викликає почуття пекучості, яке зменшується при розведенні з водою). В екстемпоральній практиці використовується для відтворення гострої ниркової недостатності.
Використовують Гліцерин в органічному синтезі (напр. хіноліну), у виробництві нітрогліцерину, гліфталевих смол, як пом’якшувач для тканин, для обробки шкіри, у виробництві паперу, у виготовленні компонентів емульгаторів, антифризів, мастил, мил, клеїв.
Допоміжні речовини та їх застосування в технології лікарських форм / За ред. Ф. Жогло. — Львів, 1996; Компендиум 2015 — лекарственные препараты / Под ред. В.Н. Коваленко. — К., 2015; Черных В.П., Зименковский Б.С., Гриценко И.С. Органическая химия / Под общ. ред. В.П. Черных. — 2-е изд. — Х., 2007.
