ФАРМАКОГЕНОМІКА (грец. pharmakon — ліки + genos — походження) — наука, що вивчає вплив генетичних чинників на особливості реакції організму на вплив ЛП. Успіхи у сфері вивчення геному людини створили наукову базу та необхідні технологічні передумови для подальшого прогресу фармакології. Внаслідок визначення послідовності нуклеотидів у молекулах ДНК (секвінування) генома людини, вдосконалення методів генетичного аналізу остаточно сформувався новий напрямок — Ф. Вона швидко розвивається, являє собою «сплав» фармакогенетики та сучасних геномних технологій. Ф. фокусує свою увагу на пошуку нових ЛП для лікування з урахуванням знань про структуру геному людини на базі вивчення генетичних основ варіабільності відповіді пацієнта на ліки, що визначається різницею у спадковій природі різних людей. Ф. вивчає також особливості будови ДНК людини, що може послабити або посилити вплив ліків; розробляє тести для вибору найбільш оптимального ЛП для лікування конкретної людини. Таким чином, Ф. можна розглядати як один із перших реальних практичних додатків до результатів, досягнених учасниками міжнародного проекту «Геном людини». Нині пошук нових ліків значною мірою відрізняється від того, що було раніше, а у майбутньому завдяки Ф. він повинен стати більш результативним.
Шляхи створення ЛП
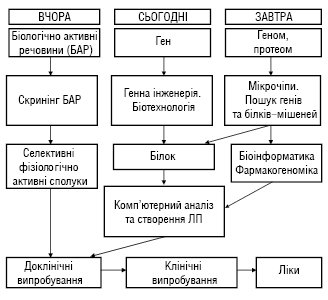
Ще не так давно великим досягненням вважалося відштовхуватися від конкретного гена, що стало дуже важливим етапом на шляху створення більш ефективних ЛП. Нині основні шляхи пошуку нових ефективних ЛП базуються на знаннях про повну структуру геному людини з переходом на знання про структуру всіх білків людини (його протеому). За всі часи секвінування геному людини було визначено лише 500 молекулярних мішеней, на які спрямовувалася дія ЛП. Тепер завдяки успіхам у питаннях геному людини очікується десятикратне збільшення кількості таких мішеней. Отже, Ф. здійснює пошук нових мішеней на базі секвенованої нуклеотидної послідовності ДНК людини та комп’ютера. За допомогою комп’ютерів здійснюється відбір серед наявних у людини мільйонів різноманітних хімічних сполук, здатних специфічно взаємодіяти з певними білками-мішенями, що визначають розвиток тієї чи іншої хвороби. Найважливіший напрямок у Ф. — перехід медицини до персоніфікованого лікування. Сьогодні вже накопичено багато інформації про гени, які впливають на процеси всмоктування, розподілу, метаболізму та виведення ЛП. У зв’язку з поліморфізмом таких генів у деяких пацієнтів ЛП можуть бути неефективними або навіть мати токсичний вплив. Напр., у нормі в різних групах досліджуваних людей швидкість видалення (елімінації) ліків з організму може відрізнятися від 4 до 100 разів. Одним із комплексів генів, що визначають метаболізм ЛП, є гени системи цитохрому Р450. Швидкість метаболізму ліків у людей з різними змінами цих генів відрізняється у сотні разів. Це вказує на те, що в окремих індивідуумів можливий розвиток побічних реакцій у відповідь на прийом ЛП навіть у звичайних дозах. Через негативні реакції на сильнодіючі ЛП щорічно у світі гине до 100 тис. осіб. Тепер фармацевтичні компанії планують використовувати всі дані Ф. для виробництва ліків, призначених для різних груп пацієнтів. Це допоможе усунути побічні реакції ліків, точніше зрозуміти механізм їх дії і таким чином знизити мільйонні витрати на пошук нових ЛП. Зокрема, генотипування лікарської стійкості зможе призвести до більш ефективної та безпечної хіміотерапії у кожного хворого на рак. На практиці лікування раку носить переважно емпіричний характер і засноване швидше на клінічних даних, ніж на розумінні механізмів чутливості до хімічних агентів. Ф. обіцяє зробити вибір потрібного препарату більш швидким та точним. Лікарі інколи не враховують вікових змін, що відбуваються в організмі в процесі старіння, і прописують пацієнтам ліки, які їм не зовсім підходять. Це ще один з аспектів Ф. Унаслідок виявлення нових генів та наступного визначення їх точних функцій буде розроблено спеціальні тести (напр. у вигляді мікрочіпів) для визначення персональних реакцій організму на різноманітні ЛП. Завдяки фармакогеномним тестам з’явиться можливість визначити вірогідність виникнення у конкретної людини побічних реакцій, що розвиваються внаслідок використання одного або групи ЛП. На мікрочіпах у недалекому майбутньому буде нанесено всі чутливі гени, що визначають типи реакції на той чи інший ЛП. Це призведе до зміни характеру фармацевтичної промисловості, коли виробники стандартної продукції та продавці «універсальних» ліків будуть пропонувати високоякісні медичні послуги, вигідні для економіки охорони здоров’я в цілому.
Ф. дозволить створити на своїй основі індивідуалізовану (персоніфіковану) медицину — медицину майбутнього, внаслідок чого підвищиться ефективність медикаментозної терапії та зменшиться кількість побічних ефектів.
Медична біологія / В.П. Пішак, Ю.І. Бажора, Ш.Б. Брагін та ін. / За ред. В.П. Пішака, Ю.І. Бажори. — Вінниця, 2004; Тарантул В.З. Геном человека: Энциклопедия, написанная четырьмя буквами. — М., 2003.
