ДИХРОМАТОМЕТРІЯ (біхроматометрія) — титриметричний метод, що базується на використанні калію дихромату як титранту-окисника для визначення відновників у кислому середовищі. При титруванні відновників дихромат відновлюється за схемою + 6e + Cr2O72- + 14H+ 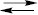
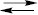 2Cr3+ + 7H2O. Стандартний електродний потенціал (E°) дорівнює + 1,33 B. Рівноважний потенціал Е згідно з рівнянням Нернста при 25 °С змінюється залежно від складу середовища від 0,93 (0,1 моль/дм3 HCl) до 1,66 В (13 моль/дм3 H3PO4).
2Cr3+ + 7H2O. Стандартний електродний потенціал (E°) дорівнює + 1,33 B. Рівноважний потенціал Е згідно з рівнянням Нернста при 25 °С змінюється залежно від складу середовища від 0,93 (0,1 моль/дм3 HCl) до 1,66 В (13 моль/дм3 H3PO4).
Титрант — водний розчин K2Cr2O7 готують як розчин первинної стандартизації за точною наважкою перекристалізованого та висушеного при 200 °С калію дихромату, концентрація якого не змінюється тривалий час і який не відновлюється Cl–-іонами та невеликими домішками органічних речовин, які наявні у дистильованій воді.
Дихромат-іони реагують з достатньою швидкістю тільки у кислому середовищі за наявності значної кількості НCl, H2SO4, H3PO4. Для визначення кінцевої точки титрування використовують внутрішні редокс-індикатори дифеніламін, дифеніламінсульфокислоту, N-фенілантранілову кислоту, а також зовнішні індикатори, напр. AgNO3, K3[Fe(CN)6], які утворюють кольорові осади із залишком титранту, або за появою кольору іонів Cr(VI).
Дихроматометрію використовують для визначення Fe(ІІ), Tl(I), W(III), Mo(III), Sn(II), Ti(III), органічних сполук (гідрохінону, аскорбінової кислоти). Можливе використання дихроматометрії для визначення хлоратів, нітратів, які попередньо відновлюють додаванням кількісно визначеного об’єму стандартного розчину Fe(ІІ). Надлишок Fe(ІІ) відтитровують K2Cr2O7 з індикаторами дифеніламіном, дифеніламіносульфокислотою (за наявності Н3РО4) або N-фенілантраніловою кислотою. Фосфорна кислота зв’язує у комплекс іони Fe(ІІІ). Цей варіант дихроматометрії має назву зворотного ферометричного титрування.
Дихроматометричне визначення катіонів таких металів, як Ag(І), Ba, Pb(II), базується на їх взаємодії з К2Cr2O7 з утворенням малорозчинних у воді хроматів (осаджувальне титрування). Кінцеву точку титрування встановлюють за допомогою зовнішнього індикатора AgNO3.
При зворотному титруванні надлишок іонів Cr2O72– після осадження хроматів відтитровують розчином солі Fe(ІІ) з фероїном як індикатором або розчином Na2S2O3 з KI та крохмалем.
Аналитическая химия / В.В. Болотов, О.М. Гайдукевич, Е.Н. Свечникова и др. — Х., 2001; Пономарев В.Д. Аналитическая химия. В 2 ч. — М., 1982. — Ч. 1, Ч. 2; Шарло Г. Методы аналитической химии. — М.–Л., 1966.
