ХРОНОФАРМАКОЛОГІЯ (грец. chrónos — час + фармакологія) — науковий напрямок, складова частина фармакології, а також хронобіології і хрономедицини, що вивчають коливальні процеси в організмі та їхній вплив на стан здоров’я. Становлення Х. — молодої сфери знання — тісно пов’язано з розвитком комплексної міждисциплінарної науки біоритмології, що сформувалася в 1960 р.
Предмет дослідження Х. — залежність дії ЛП від чинника часу, стану біоритмічних процесів і, з іншого боку, оцінка впливу ліків на коливальні явища в живих системах. Ці відомості необхідні для оптимізації фармакотерапії. У сучасних умовах подальший прогрес фармакології неможливий без урахування чинника часу, оскільки будь-яке фармакологічне втручання перебудовує ті чи інші біологічні ритми, а самі вони обумовлюють мінливість фармакологічного ефекту. Ритмічні коливання, тобто циклічні зміни інтенсивності біологічних процесів, притаманні будь-яким формам життя на всіх його рівнях — від клітинного до організменого. Біологічний сенс таких коливань полягає в адаптації до періодичних змін стану навколишнього середовища (освітленості, температури, атмосферного тиску та ін.) і в захисті біологічної системи від надмірного виснаження. Припинення коливань призводить до загибелі організму. Існує велика кількість біоритмів з періодом від частки секунди до десятків років (див. Біологічні ритми). Найбільш вивчені навколодобові, або циркадіанні ритми (від лат. circa — навколо, біля + dies — день) з періодом коливань близько 24 год (у межах 20–28 год). Описано вже більше 300 фізіологічних показників із подібним періодизмом. Відомі також коливання з більш високими частотами — навкологодинні (ультрадіанні), хвилинні, секундні — та коливання з більш низькими частотами — інфрадіанні (тижневі, місячні), сезонні та ін. На вираженість фармакологічних ефектів найбільше впливають циркадіанні, місячні та сезонні ритми. Прикладами циркадіанних біоритмів є цикли сну — не сну, ритмічні зміни температури тіла, АТ, частоти поділу клітин та ін. Приклади місячних біоритмів — оваріально-менструальний цикл у жіночому організмі й менш жорстко детерміновані циклічні зміни гормонального фону, вегетативних показників, емоційного стану, фізичної працездатності в чоловіків.
Ритми з тривалим періодом контролюються переважно екзогенними чинниками — зміною геофізичних параметрів внаслідок обертання Землі навколо своєї осі та навколо Сонця, але мають значення й ендогенні впливи. Напр., навіть в умовах світло- і звукоізоляції не виникає кардинальної зміни 24-годинного ритму; у зрізах надниркових залоз, що культивуються, зберігається циркадіанний ритм секреції кортикостероїдів. Ритми з коротким періодом контролюються переважно ендогенними факторами.
Управління біоритмами реалізується на центральному і периферичному рівнях з переважним значенням центрального. Центральні механізми, що задають і організують ритми, локалізовані в головному мозку. Первинним водієм ритму є супрахіазматичні ядра гіпоталамуса, активність яких залежить від рівня освітленості і співвідношення світлого й темного часу доби. Ці ядра тісно зв’язані з зоровим аналізатором, із шишкоподібною залозою проміжного мозку — епіфізом, у якому синтезується мелатонін, а також зі смугастим тілом (контролює моторику і психічні процеси), гіпокампом (контролює емоційний статус), іншими ядрами гіпоталамуса (регулюють діяльність периферичних залоз внутрішньої секреції і вегетативний статус).
У кожному біологічному ритмі виділяється період — тривалість циклу, амплітуда — розмах між граничними значеннями ритмічно повторюваного процесу, акрофаза — граничне відхилення процесу, що реєструється, зона блукання фази — діапазон відхилень положення акрофази в повторних визначеннях, мезор — середнє значення показника, що характеризує рівень функціонування біологічної системи (рисунок). Численні ліки здатні змінювати ці параметри. Результатом такого втручання в ідеальному випадку стає усунення патологічної ритмічності, що сприяє видужанню. Класичним прикладом є розроблена ще І.П. Павловим методика лікування неврозів комбінацією речовин з різною спрямованістю дії на ЦНС — седативною (броміди) і психостимулювальною (кофеїн), що дозволяє дестабілізувати патологічний ритм. Давно відома й практика застосування пірогенних препаратів, що навмисно загострюють запальні процеси із млявим перебігом. Із хронофармакологічних позицій таке втручання, що сприяє включенню захисних механізмів, відновлює коливальний режим, близький до нормального. З іншого боку, небажаним ефектом ліків може бути й нав’язування організму нового стану — фармакогенного ритму, що сам по собі здатний стати джерелом патології.
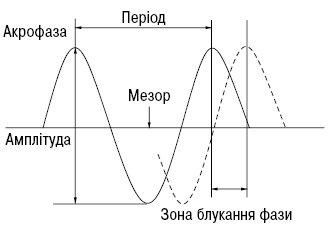
Рисунок. Параметри біоритму (за Е.Б. Арушаняном)
Ефект ліків завжди нестаціонарний, зазнає коливань. Хронологічний аспект фармакодинаміки має назву хронестезія (ритмічні зміни чутливості до ліків у часі), фармакокінетики — хронокінетика (залежність фармакокінетичних параметрів від чинника часу). Звичайно найбільш виражений ефект ліків протягом доби припадає на період максимальної активності організму (у людей удень, у нічних тварин, напр. щурів, уночі). Напр., у людини пік дії сечогінних препаратів спостерігається в першій половині дня. У пацієнтів із серцевою недостатністю фуросемід чинить максимальний діуретичний ефект о 10:00–11:00, а о 13:00 препарат викликає більш виражену втрату калію, частіше виявляється побічна дія. Хронокінетична особливість діазепаму — досягнення максимальної концентрації речовини в крові при введенні стандартної дози препарату в ранкові години, тоді як при введенні ввечері концентрація транквілізатору в крові значно нижча.
ЛП здатні змінювати індивідуальне сприйняття часу. Так, антидепресанти при психічній депресії нормалізують тривалість індивідуальної хвилини, що можна використовувати як зручний діагностичний критерій при оцінюванні тяжкості захворювання й ефективності фармакотерапії. Кофеїн у стандартній дозі 200 мг у здорових добровольців скорочує індивідуальну хвилину, особливо на тлі стомлення. Барбітурати, седативні засоби, як правило, сповільнюють сприйняття часу. Адаптогенні препарати, такі як елеутерокок, аралія, мають регулювальну дію: якщо вихідна тривалість індивідуальної хвилини скорочена, курсове застосування цих препаратів подовжує її, якщо подовжена — скорочує.
Будь-якій формі патології притаманне ламання біоритмів. У механізмах розвитку численних патологічних станів і захворювань бере участь значна фазова неузгодженість біоритмів окремих фізіологічних функцій — десинхроноз. Найбільш типові такі його прояви, як зниження розумової й фізичної працездатності, вегетативні порушення, психічна пригніченість, порушення сну, дратівливість, зниження апетиту. Хронобіологічний дефект, що виник під впливом різних чинників, обумовлює розвиток або підтримку вже існуючого патологічного процесу. У практичному відношенні важливо, що одночасне застосування великої кількості ЛП (поліпрагмазія) сприяє неузгодженості біоритмів, появі десинхронозу, що може опосередковувати побічну дію ліків. Ресинхронізації біоритмів й усуненню десинхронозу сприяють препарати з адаптогенними властивостями — як рослинного походження, так і синтетичні, зокрема дибазол (див. Адаптогени), а також полівітамінні ЛП. Доцільне сполучення прийому цих препаратів з дією факторів, що синхронізують біоритми, — дотриманням режиму харчування, праці й відпочинку, світлового режиму.
Урахування чинника часу, тривалості світлого й темного періоду доби важливе в організації фармакологічних і токсикологічних експериментів, оскільки відсутність стандартних умов, постановка дослідів у різний час доби є джерелом поганої відтворюваності результатів, а іноді навіть їх протилежного характеру. Напр., летальний ефект токсичних доз фенобарбіталу протягом доби коливається від 0 до 100%.
Природним клінічним продовженням Х., реалізацією її положень на практиці є хронофармакотерапія. Вона дозволяє підвищити ефективність лікування і зменшити кількість і вираженість побічних ефектів. Початок сучасної хронофармакотерапії було покладено в 50-ті роки ХХ ст., коли хворим з недостатністю функції кори надниркових залоз запропонували вводити препарати глюкокортикоїдних гормонів рано вранці. Рекомендація обґрунтовувалася даними про те, що в цей час чутливість рецепторів до відповідних гормонів найбільш висока. Така тактика дозволила не тільки підвищити ефективність лікування, але й зменшити побічну дію у вигляді атрофії власних надниркових залоз внаслідок негативного зворотного зв’язку. АКТГ, навпаки, доцільно вводити пізно ввечері, оскільки його стимулювальний вплив на надниркові залози розвивається після півночі й до ранку досягає максимуму.
Досить глибоко досліджені хронобіологічні особливості серцево-судинних захворювань. У багатьох пацієнтів, що страждають на гіпертонічну хворобу, максимальне підвищення АТ відбувається у вечірні години. Тому в таких випадках доцільний прийом антигіпертензивних препаратів тривалої дії (дигідропіридинових блокаторів кальцієвих каналів — амлодипіну, лацидипіну та ін., інгібіторів АПФ — лізиноприлу, еналаприлу, периндоприлу та ін.) увечері, тобто напередодні підвищення АТ. Це ж стосується клофеліну, стійкий гіпотензивний ефект якого при традиційному прийомі 3 рази на добу звичайно розвивається на другому тижні лікування, а при одноразовому застосуванні ввечері — вже на першому. До того ж частота численних і звичайно погано переносимих побічних ефектів клофеліну при хронофармакологічному режимі застосування в 6 разів нижча, ніж при традиційному. Введення блокаторів Н1-гістамінових рецепторів рано вранці забезпечує приблизно вдвічі більш тривалий протиалергічний ефект, ніж при введенні ввечері. Побічні алергічні реакції, зокрема на введення антибіотиків, частіше зустрічаються при їхньому використанні ввечері, що пов’язано з нерівномірним утворенням медіатора алергічних реакцій негайного типу гістаміну протягом доби з максимумом у вечірній час.
Використання принципів Х. ефективно й в інших сферах медицини. Зокрема, в психіатрії використання трициклічних антидепресантів 1 раз на добу (опівночі) забезпечує більш швидкий терапевтичний ефект, ніж прийом в інший час або розподіл дози протягом дня. В онкології особливо бажаною є максимальна дія цитостатиків на піку найвищої мітотичної активності пухлинних клітин, коли вони найбільш чутливі до дії ліків. Для лейкемічних клітин це друга половина світлового дня. Відомі приклади більш швидкого настання ремісії в дітей з гострим лейкозом при введенні цитостатиків о 14:00 та 19:00, ніж при рівномірному розподілі добової дози протягом дня. У хворих на рак легень хронофармакологічне призначення метотрексату (о 18:00, 21:00, 24:00, 03:00) сприяє значно більш частому досягненню ремісії, більшій виживаності й зниженню частоти побічних ефектів порівняно з шаблоновим режимом хіміотерапії, коли добова доза розподіляється рівномірно.
Подальший розвиток Х. і хронофармакотерапії, застосування їхніх досягнень на практиці є потужним чинником підвищення ефективності й безпеки фармакотерапії. Можна вважати за доцільне включення хронофармакологічних рекомендацій, що накопичуються, до спеціальних видань, анотацій до ЛП і стандартів лікування.
Арушанян Э.Б. Хронофармакотерапия заболеваний // Эксперим. и клин. фармакол. — 1992. — № 2; Арушанян Э.Б. Хронофармакология. — Ставрополь, 2000; Маркова И.В., Неженцев М.В. Фармакология. — СПб., 1997; Харкевич М.Д. Фармакология. — М., 2001; Lemmer B., Labrecque G. Chronopharmacology and chronoterapeutics. Definitions and concepts // Chronobiol. Int. — 1987. — Vol. 4, № 3.
