ЕКСТРАКЦІЯ В АНАЛІТИЧНІЙ ХІМІЇ — універсальний, простий експресний метод фазового розподілу та концентрування основних компонентів, що аналізують. Його широко використовують в аналітичній хімії з метою селективного добування елементів із сумішей для кількісного визначення та встановлення вмісту домішок у сполуках, що дуже важливо при одержанні особливо чистих речовин. При рідинній екстракції відбувається рівноважний розподіл компонентів між рідинними фазами, які не змішуються, напр. водною та органічною. Екстракція неелектролітів не супроводжується хімічними реакціями і відбувається за механізмом фізичного розподілу. Кількісна характеристика цього процесу — коефіцієнт розподілу σ, який розраховується за законом розподілу Нернста. У випадку екстракції електролітів, які дисоціюють у водній фазі, можливий перебіг реакцій приєднання за сольватним або гідратно-сольватним механізмом катіонного або аніонного обміну, а також можливі різні комбінації цих процесів. При цьому між екстрагентом та речовиною, що екстрагують, утворюється відносно стійкий зв’язок (40–200 кДж/моль). Розчинники, які не сольватують речовину, що екстрагується, або мають невелику здатність до сольватації, належать до інертних. Це бензол (С6H6), толуол (С6H5СH3), тетрахлорид карбону (ССl4), хлороформ (CHCl3), нітробензол (C6H5NO2), хлорбензол (C6H5Cl) та ін. Екстракцію за механізмом фізичного розподілу використовують для попереднього концентрування при визначенні органічних сполук, розчинених у воді, при аналізі природних та стічних вод, забруднених нафтопродуктами та іншими домішками органічного походження. Класичним прикладом такого виду екстракції є отримання йоду з багатьох сумішей. До активних екстрагентів належать розчинники, в молекулах яких міститься оксиген: спирти (бутанол С4Н9ОН та ін.), прості ефіри (діетиловий ефір С2Н5ОС2Н5), кетони (циклогексанон (СН2)5СО, пентанон (С2Н5)2СО, метилетилкетон СН3СОС2Н5), естери (етилацетат СН3СООС2Н5, трибутилфосфат О=Р(ОС4Н9)3, дибутилфосфат 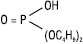 тощо).
тощо).
Ці розчинники екстрагують мінеральні (HCl, HBr, HI, HNO3, HClO4, H2SO4), комплексні (HFeCl4, HInI4, HSbCl6) кислоти, гетерополікислоти арсену H3[As(Mo3O10)4], фосфору H3[P(Mo3O10)4], кремнію H3Si(Mo3O10)4, які найчастіше використовують в аналізі для визначення домішок As, P, Si. Сполуки, у вигляді яких елементи переходять у шар органічного розчинника, можуть утворюватися в процесі власне екстракції активними розчинниками за рахунок взаємодії реагенту, що входить до складу органічної фази, з катіонами металів водної фази. Це хелатні сполуки катіонів металів з різними органічними реагентами, які мають функціонально-аналітичні угруповання з донорно активними атомами оксигену, сульфуру, нітрогену, напр. β-дикетони, оксими, нітрозофеноли, азосполуки, ксантогенати. Так, дифенілтіокарбазон (дитизон) використовують в екстракційно-фотометричному визначенні срібла, меркурію, купруму, плюмбуму, цинку. Для визначення багатьох катіонів використовують екстракцію іонних асоціатів, які є солями, утвореними великими катіонами й аніонами. Іонні асоціати беруть участь у процесі сольватації органічними розчинниками і переходять в органічну фазу. До великих катіонів належать катіони тетрафеніларсонію (C6H5)4As+, тетрафенілфосфонію (C6H5)4P+, комплексні катіони лужних, лужноземельних та інших металів з макроциклічними лігандами (краун-етерами). Великі однозарядні аніони неорганічних кислот (ClO4-, ReO4- та ін.) утворюють іонні асоціати з катіонами тетрафеніларсонію, комплексними катіонами металів. Кількісний опис екстракційної рівноваги електролітів засновано на використанні закону діючих мас стосовно кожного випадку екстракції. Знання рівнянь екстракції дозволяє обрати умови добування, розподілу та концентрування. У фармацевтичному аналізі широко застосовують екстракційно-фотометричний метод визначення ЛП, що базується на утворенні ними іонних асоціатів з різними реагентами, які екстрагуються органічним розчинником. При цьому як реагенти для органічних катіонів часто використовують барвники кислотного характеру, напр. метиловий оранжевий, а для органічних аніонів барвники основного характеру, напр. родамін 6Ж.
Коренман И.М. Экстракция в анализе органических веществ. — М., 1977; Москвин Л.Н., Царицина Л.Г. Методы разделения и концентрирования в аналитической химии. — Л., 1991; Пилипенко А.Т., Пятницкий И.В. Аналитическая химия: В 2 кн. — М., 1990.
